La química de la vida
"EXTRACCION DE ADN"
PROCEDIMIENTO:
Ordenadores de la secuencia
Banco de recursos
"EXTRACCION DE ADN"
OBJETIVOS:
Utilizar técnicas sencillas para poder extraer ADN de un vegetal. Observar la estructura fibrilar del ADN, a simple vista y en el microscopio.
Registrar todos los pasos y resultados.
FUNDAMENTO:
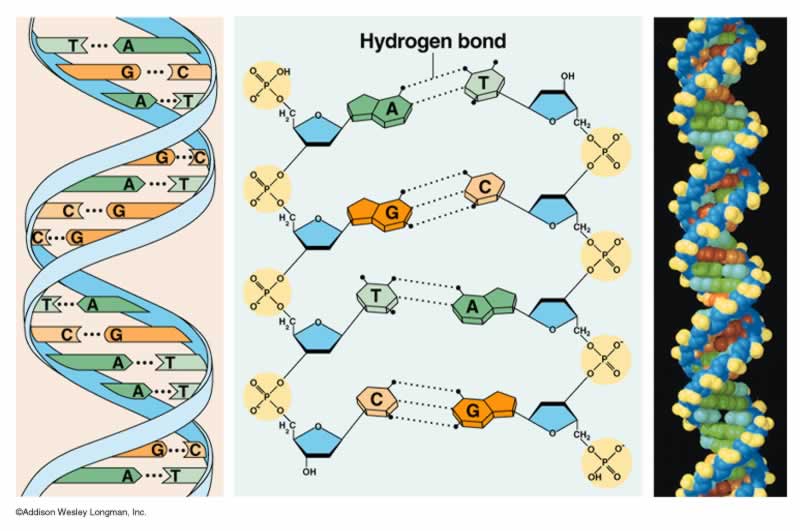
El ADN (ácido desoxirribonucléico) constituye el material genético de los organismos.
Para realizar este experimento es necesario moler el vegetal por algún procedimiento mecánico, con el fin de disgregar primero las células de los tejidos y luego romper algunas de ellas. Se empieza por Usar (romper) la pared celular y la membrana plasmática para poder acceder al núcleo de la célula.
A continuación debe romperse también la membrana nuclear para dejar libre al ADN.
Los jabones y detergentes emulsionan los lípidos de las membranas celulares y las rompen.
La sal evita la unión de las proteínas al ADN.
Para aislar el ADN hay que hacer que precipite en alcohol. El ADN es soluble en agua, pero cuando se encuentra en alcohol se desenrolla y precipita en la interfase entre el alcohol y el agua.
Además de permitirnos ver el ADN, el alcohol separa el ADN de otros componentes celulares, los cuales son dejados en la solución acuosa.
Al aglutinarse, el ADN forma partículas macroscópicas y se hace visible (tenga en cuenta que son agregados de millones de millones de millones de moléculas de la doble hélice del ADN).
MATERIALES:
2 vasos de precipitados, 3 tubos de ensayo, varilla de vidrio, mortero, colador,, micro pipeta, cucharita, ansa o palillo de madera. Agua destilada, sal, detergente, Pepsina (enzima), alcohol etílico a 0° C. Material vegetal (banana, arvejas, hojas de espinaca, etc). Sacarosa.
PROCEDIMIENTO:
Cortar media banana en trozos y colocarlos en el mortero. Molerlos bien.
Agregar poco a poco 120 mil de agua destilada con una cucharadita de sal disuelta. Moler y mezclar bien hasta consistencia homogénea.
Pasar la mezcla a un vaso de precipitado y añadir 2 cucharaditas de detergente. Agitar suavemente para que no se forme espuma.
Colar la mezcla.
Añadir al filtrado una pizca de Pepsina (enzima). Agitar durante 5 minutos.
Colocar en 5 tubos de ensayo 5 mil del líquido filtrado.
Agregar a cada tubo 5 mil de alcohol Etílico a 0°C dejándolo escurrir lentamente por las paredes del tubo, para ello utilizar una pipeta. Dejar reposar los tubos y observar. El ADN se elevará desde la solución acuosa hasta la capa de alcohol y quedará en la interfase. El ADN prefiere la capa superior, el alcohol. El ADN es una larga y pegajosa molécula a la que le gusta formar grumos.
Registrar la experiencia y ordenarla en una secuencia Power Point, que incluya las conclusiones.
Ordenadores de la secuencia
1. ¿Por qué se usa detergente? ¿Cómo funciona el detergente?
2. El ananá posee una enzima que rompe las proteínas, ¿por qué es necesario usarla?
3. La cosa blanca y pegajosa, ¿es una mezcla de ADN y ARN?
4. ¿A qué grupo de sustancias químicas pertenecen el ARN y el ADN?
5. Describir brevemente al ADN y ARN.
6. ¿Cuál es la función de cada uno? Relacionar con las leyes de transmisión de los caracteres hereditarios (mendelianas y no mendelianas?
7. En una mutación genética ¿qué es lo que cambia?
8. En una patología cromosómica, ¿qué se alteró?
9. Completa el Power Point, utilizando los recursos que figuran a continuación
Banco de recursos
Segunda parte
Actividad 1: interpretación, investigación
1. Redactar un texto que explique el cuadro. (Ampliar el significado de los términos)
1. Redactar un texto que explique el cuadro. (Ampliar el significado de los términos)
Recursos: Video sobre adn, ESTRUCTURA Y EVOLUCIÓN
Recursos: Video sobre la trascripción.
http://www.educ.ar/sitios/educar/recursos/ver?id=105156&referente=docentes
http://videos.educ.ar/play/Disciplinas/_Biologia/Transcripcion_del_ADN
http://videos.educ.ar/play/Disciplinas/_Biologia/ADN
http://videos.educ.ar/play/Disciplinas/_Biologia/Duplicacion_del_ADN
Leer este artículo:
http://mqciencia.com/2011/05/10/rosalind-franklin-un-espiritu-inquebrantable/

Actividad:
mayores méritos no significan necesariamente mayor reconocimiento.
http://videos.educ.ar/play/Disciplinas/_Biologia/Transcripcion_del_ADN
http://videos.educ.ar/play/Disciplinas/_Biologia/ADN
http://videos.educ.ar/play/Disciplinas/_Biologia/Duplicacion_del_ADN
http://videos.educ.ar/play/Disciplinas/_Biologia/ADN
http://videos.educ.ar/play/Disciplinas/_Biologia/Duplicacion_del_ADN

http://mqciencia.com/2011/05/10/rosalind-franklin-un-espiritu-inquebrantable/

Actividad:
mayores méritos no significan necesariamente mayor reconocimiento.
Luego de leer el texto argumentar en dos o tres párrafos la frase anterior.
-Video sobre la duplicación del ADN.

 Cuando una célula se divide y da como resultado dos células hijas, cada una de éstas recibe una molécula de ADN idéntica a la de la célula madre. En consecuencia, una molécula de ADN ha de duplicarse durante la división celular, generando una copia idéntica a ella, es decir, con la misma secuencia de bases.
Este proceso es el GAP "S"o de síntesis del ciclo celular. antes de la meiosis o mitosis.
Recordar:
Cuando una célula se divide y da como resultado dos células hijas, cada una de éstas recibe una molécula de ADN idéntica a la de la célula madre. En consecuencia, una molécula de ADN ha de duplicarse durante la división celular, generando una copia idéntica a ella, es decir, con la misma secuencia de bases.
Este proceso es el GAP "S"o de síntesis del ciclo celular. antes de la meiosis o mitosis.
Recordar:


Cuando una célula se divide y da como resultado dos células hijas, cada una de éstas recibe una molécula de ADN idéntica a la de la célula madre. En consecuencia, una molécula de ADN ha de duplicarse durante la división celular, generando una copia idéntica a ella, es decir, con la misma secuencia de bases.
Este proceso es el GAP "S"o de síntesis del ciclo celular. antes de la meiosis o mitosis.
Recordar:
 El ADN forma en el núcleo una sustancia llamada cromatina que tiene contacto con proteínas de diferente tipo.Según el grado de condensación de la cromatina pueden transcribirse diferentes genes o, no transcribirse.Cuando la célula se duplica, el ADN se duplica y se condensa o superenrolla antes de la mitosis o meiosis, y se condensa en cuerpos mas fáciles de dividir: los cromosomas.
El ADN forma en el núcleo una sustancia llamada cromatina que tiene contacto con proteínas de diferente tipo.Según el grado de condensación de la cromatina pueden transcribirse diferentes genes o, no transcribirse.Cuando la célula se duplica, el ADN se duplica y se condensa o superenrolla antes de la mitosis o meiosis, y se condensa en cuerpos mas fáciles de dividir: los cromosomas.
Dado que el ADN es una molécula relativamente inerte, su información se expresa indirectamente, a través de otras moléculas. El ADN dirige la síntesis de proteínas y éstas determinan las características físicas y químicas de la célula.
Podemos pensar al código genético como un idioma. Los idiomas utilizan una cierta cantidad de letras, éstas se combinan para formar palabras, y cada palabra tiene un significado, designa a un objeto particular. En el código genético están presentes todos estos elementos: las letras son las 4 bases que forman las cadenas de ARN (A, U, C, G); las palabras son siempre agrupaciones de 3 letras o tripletes de bases, llamadas codones en la molécula del ARNm, y los objetos designados por dichas palabras son cada uno de los 20 aminoácidos que componen las proteínas.
- El código genético consta de 64 codones o tripletes de bases.61 codones codifican aminoácidos.
- 3 codones funcionan como señales de terminación.
- El código no es ambiguo, pues cada codón especifica a un solo aminoácido.
- El código es degenerado, ya que un aminoácido puede estar codificado por diferentes codones.
- Es universal, debido a que sus mensajes son interpretados de la misma forma por todos los organismos.
- Utiliza un marco de lectura establecido al inicio de la traducción y no lo modifica.
- No se produce solapamiento de codones.
El ADN lleva toda la información necesaria para que los seres vivos fabriquen las moléculas que constituyen sus células y tejidos. Estas moléculas están formadas por cadenas de aminoácidos, y las llamamos proteínas.
Dado que el ADN es una molécula relativamente inerte, su información se expresa indirectamente, a través de otras moléculas. El ADN dirige la síntesis de proteínas y éstas determinan las características físicas y químicas de la célula.
Como ya adelantáramos, las instrucciones genéticas contenidas en el ADN se expresan en dos pasos. El primero de ellos, la transcripción, consiste en la síntesis de ARN a partir del ADN. El ARN contiene toda la información de la secuencia de bases del ADN de la que ha sido copiado. El segundo paso de la expresión genética es la traducción, momento en el cual el ARN ejecuta las instrucciones recibidas cristalizándolas en la síntesis de una proteína específica.
Existen diversos tipos de ARN: el ARNm (mensajero), el ARNr (ribosómico), el ARNt (de transferencia) y los ARN pequeños. De todos ellos, tan sólo el ARNm es portador de información acerca de la secuencia aminoacídica de una proteína; sin embargo todos ellos son transcriptos de ADN. Por lo tanto, resulta necesario revisar la segunda definición del gen.
Hoy se acepta que un gen es una secuencia de ADN transcripta que genera un producto con función celular específica.
Cabe aclarar, no obstante, que esta definición no es completamente satisfactoria, en la medida en que existen regiones reguladoras de los genes, que no se transcriben, y otras regiones (llamadas intrones) que se transcriben pero se eliminan sin cumplir ninguna función aparente.
Transcripción y traducción: Video
Podemos pensar al código genético como un idioma. Los idiomas utilizan una cierta cantidad de letras, éstas se combinan para formar palabras, y cada palabra tiene un significado, designa a un objeto particular. En el código genético están presentes todos estos elementos: las letras son las 4 bases que forman las cadenas de ARN (A, U, C, G); las palabras son siempre agrupaciones de 3 letras o tripletes de bases, llamadas codones en la molécula del ARNm, y los objetos designados por dichas palabras son cada uno de los 20 aminoácidos que componen las proteínas.
¿Por qué las palabras-codones se forman con 3 bases? Si cada palabra constara de 1 base, habría 4 palabras, y si se formara con 2, las palabras posibles serían 16. En ninguno de los casos alcanzarían para designar a todos los aminoácidos. Pero se pueden obtener 64 combinaciones diferentes si las bases se combinan de a 3; 64 codones son más que suficientes para nombrar a los 20 aminoácidos.
Los codones que codifican aminoácidos suman en total 61. Los 3 codones que no especifican ningún aminoácido, UGA, UAG y UAA, actúan como señales de terminación en la traducción o síntesis de proteínas. Son llamados codones de terminación o stop.
La tabla del código que se halla a continuación es válida para los seres vivos más diversos: el hombre, las bacterias, las levaduras, las plantas. El código genético es universal, lo cual da prueba de que todos los organismos comparten un mismo origen. Una de las contadas excepciones a la universalidad del código es el ADN mitocondrial, en el cual algunos codones son leídos de manera diferente.
Características del Código Genético
- El código genético consta de 64 codones o tripletes de bases.61 codones codifican aminoácidos.
- 3 codones funcionan como señales de terminación.
- El código no es ambiguo, pues cada codón especifica a un solo aminoácido.
- El código es degenerado, ya que un aminoácido puede estar codificado por diferentes codones.
- Es universal, debido a que sus mensajes son interpretados de la misma forma por todos los organismos.
- Utiliza un marco de lectura establecido al inicio de la traducción y no lo modifica.
- No se produce solapamiento de codones.
El ADN lleva toda la información necesaria para que los seres vivos fabriquen las moléculas que constituyen sus células y tejidos. Estas moléculas están formadas por cadenas de aminoácidos, y las llamamos proteínas.
Las células de un solo individuo, comparten el mismo genoma, pero cada grupo celular es diferente, ¿por qué?...
RESUMEN DE LOS MECANISMOS DE REGULACIÓN GÉNICA EN EUCARIOTAS
Control transcripcional
A- Factores de transcripción
Control transporte del ARNm
Mecanismos que determinan si el ARNm maduro sale o no a citosol
Control traduccional
Mecanismos que determinan si el ARNm presente en el citosol es o no traducido
Control de la degradación del ARNm
Mecanismos que determinan la supervivencia del ARNm en el citosol
Control de la actividad proteica
Mecanismos que determinan la activación o desactivación de una proteína, como así también el tiempo de supervivencia de la misma.
ACTIVIDADES
a. Completar los recuadros blancos del dibujo con los siguientes rótulos: ADN, ARNm, RIBOSOMA, PROTEÍNA, TRADUCCIÓN, REPLICACIÓN, TRANSCRIPCIÓN.
b. Completar:
La información genética se encuentra codificada en el _____1.
Esta molécula de gran tamaño se encuentra en el ________________2 de las células _____________3 (como plantas, hongos y animales).
La forma en que la información se encuentra codificada es igual en todos los organismos, por eso se dice que el código genético es _____________4.
Cuando una célula debe dividirse para reproducirse (tanto por mitosis como por meiosis) el ADN previamente se ______________5.
Cuando una molécula de ADN se super-enrolla durante la mitosis o meiosis, puede ser vista a microscopio óptico con forma de X, esta estructura se denomina _______________6
En cada molécula de ADN se encuentran muchos genes. En términos generales, se define gen como la porción de ADN que codifica para una ______________7
Para que cada gen se exprese, deben ocurrir dos procesos: el primero consiste en la síntesis del ______8 que llevará el mensaje del ADN; este proceso se denomina ________________9. El segundo proceso consiste en la síntesis de la _____________10 respectiva en los _________11 , proceso en el cual interviene también otro ________12 conocido como _______________13 que tiene un anticodón y el aminoácido correspondiente. Este proceso se denomina _____________14.
Un cambio en la secuencia del ADN se denomina _______________15.
La expresión del ADN en cada una de las células del cuerpo es _________________16 ya que se encuentra regulada por diferentes factores:______________________________________________________________________________________________________________________________________________________17
c. Indicar qué es lo que se observa en la figura y cómo se llaman las partes numeradas.
d. Diseño de una Red conceptual con Cmap
Esta actividad consiste en dar una lista de conceptos principales y unirlos en una red que debe seguir ciertas reglas:
1.
Se debe unir de a dos conceptos por vez. Es decir que al terminar la red se pueden aislar dos conceptos y deben formar una frase coherente, que se inicia en uno de los conceptos y termina en el otro, siguiendo la dirección que indica la flecha.
2.
Todos los conceptos deben formar parte de la red (no pueden quedar conceptos sueltos), y de cada concepto pueden salir o entrar más de una flecha.
3.
En las frases empleadas para unir conceptos no se pueden repetir los conceptos principales dados por el docente. Tampoco usar expresiones como “el mismo” ya que es una forma de reiterar un concepto.
4.
No se puede usar la negación (“no”) en las frases que unen conceptos ya que la idea es demostrar conocimientos mediante la afirmación.
5.
Evitar en las frases que unen conceptos el empleo reiterado de términos tales como “es”, “tiene”, “está”. Aunque estos términos pueden ser correctos, se pretende de los alumnos que puedan redactar una frase breve y más precisa, que manifieste ideas más exactas.
A continuación se presenta una lista de conceptos y se muestra un modelo de red conceptual que se podría diseñar a partir de estos conceptos:
MUTACIONES - BIODIVERSIDAD - SERES VIVOS - ADN - EUCARIOTAS - NUCLEÓTIDOS TRANSCRIPCIÓN – GEN – ADENINA – PROTEÍNA – RIBOSOMAS – AMINOÁCIDOS BIOTECNOLOGÍA MODERNA.
e. PREGUNTAS con OPCIÓN
Control transcripcional
|
A- Factores de transcripción
B- Grado de condensación de la cromatina - eucromatina (activa) y heterocromatina (inactiva)
C- Grado de metilación
GRADO DE METILACIÓN (CH3) EL METILO INHIBE LA TRANSCRIPCIÓN SI SE ENCUENTRA EN EL CODON PROMOTOR C,G.
|
Control transporte del ARNm
|
Mecanismos que determinan si el ARNm maduro sale o no a citosol
|
Control traduccional
|
Mecanismos que determinan si el ARNm presente en el citosol es o no traducido
|
Control de la degradación del ARNm
|
Mecanismos que determinan la supervivencia del ARNm en el citosol
|
Control de la actividad proteica
|
Mecanismos que determinan la activación o desactivación de una proteína, como así también el tiempo de supervivencia de la misma.
|
ACTIVIDADES
a. Completar los recuadros blancos del dibujo con los siguientes rótulos: ADN, ARNm, RIBOSOMA, PROTEÍNA, TRADUCCIÓN, REPLICACIÓN, TRANSCRIPCIÓN.
Cuando una célula debe dividirse para reproducirse (tanto por mitosis como por meiosis) el ADN previamente se ______________5.
Cuando una molécula de ADN se super-enrolla durante la mitosis o meiosis, puede ser vista a microscopio óptico con forma de X, esta estructura se denomina _______________6
En cada molécula de ADN se encuentran muchos genes. En términos generales, se define gen como la porción de ADN que codifica para una ______________7
Para que cada gen se exprese, deben ocurrir dos procesos: el primero consiste en la síntesis del ______8 que llevará el mensaje del ADN; este proceso se denomina ________________9. El segundo proceso consiste en la síntesis de la _____________10 respectiva en los _________11 , proceso en el cual interviene también otro ________12 conocido como _______________13 que tiene un anticodón y el aminoácido correspondiente. Este proceso se denomina _____________14.
Un cambio en la secuencia del ADN se denomina _______________15.
La expresión del ADN en cada una de las células del cuerpo es _________________16 ya que se encuentra regulada por diferentes factores:______________________________________________________________________________________________________________________________________________________17
c. Indicar qué es lo que se observa en la figura y cómo se llaman las partes numeradas.
d. Diseño de una Red conceptual con Cmap
Esta actividad consiste en dar una lista de conceptos principales y unirlos en una red que debe seguir ciertas reglas:
1.
|
Se debe unir de a dos conceptos por vez. Es decir que al terminar la red se pueden aislar dos conceptos y deben formar una frase coherente, que se inicia en uno de los conceptos y termina en el otro, siguiendo la dirección que indica la flecha.
|
2.
|
Todos los conceptos deben formar parte de la red (no pueden quedar conceptos sueltos), y de cada concepto pueden salir o entrar más de una flecha.
|
3.
|
En las frases empleadas para unir conceptos no se pueden repetir los conceptos principales dados por el docente. Tampoco usar expresiones como “el mismo” ya que es una forma de reiterar un concepto.
|
4.
|
No se puede usar la negación (“no”) en las frases que unen conceptos ya que la idea es demostrar conocimientos mediante la afirmación.
|
5.
|
Evitar en las frases que unen conceptos el empleo reiterado de términos tales como “es”, “tiene”, “está”. Aunque estos términos pueden ser correctos, se pretende de los alumnos que puedan redactar una frase breve y más precisa, que manifieste ideas más exactas.
|
A continuación se presenta una lista de conceptos y se muestra un modelo de red conceptual que se podría diseñar a partir de estos conceptos:
MUTACIONES - BIODIVERSIDAD - SERES VIVOS - ADN - EUCARIOTAS - NUCLEÓTIDOS TRANSCRIPCIÓN – GEN – ADENINA – PROTEÍNA – RIBOSOMAS – AMINOÁCIDOS BIOTECNOLOGÍA MODERNA.
MUTACIONES - BIODIVERSIDAD - SERES VIVOS - ADN - EUCARIOTAS - NUCLEÓTIDOS TRANSCRIPCIÓN – GEN – ADENINA – PROTEÍNA – RIBOSOMAS – AMINOÁCIDOS BIOTECNOLOGÍA MODERNA.
e. PREGUNTAS con OPCIÓN
Sus células epiteliales y musculares son diferentes porque cada célula:
a- contiene diferentes clases de genes
b- expresa diferentes genes
c- contiene diferente número de genes
d- ha sufrido diferentes mutaciones.
El sitio de unión de la ARN pol al molde de ADN se denomina:
a- regulador
b- codificador
c- operador
d- promotor
Durante la traducción, es característico de la etapa de iniciación el acoplamiento de:
a- el codón con el anticodón iniciador
b- la subunidad mayor con la subunidad menor
c- el ARNm con la subunidad menor
d- todas son correctas
El código genético es:
a- degenerado, ambiguo y solapado
b- no degenerado, no ambiguo, no solapado
c- degenerado, no ambiguo, no solapado
d- degenerado, ambiguo, no solapado
¿Cuál de las siguientes secuencias establece un orden decreciente de estructuras?:
a- gen- cromosoma- nucleótido- codón
b- cromosoma- gen- codón- nucleótido
c- nucleótido- cromosoma- gen- codón
d- gen- cromosoma- codón- nucleótido
Segunda parte
Las proteínas determinan la forma y la estructura de las células y dirigen casi todos los procesos vitales. Las funciones de las proteínas son específicas de cada una de ellas y permiten a las células mantener su integridad, defenderse de agentes externos, reparar daños, controlar y regular funciones.
La estructura secundaria describe el modo en que una cadena peptídica se pliega o enrolla en el espacio. Muchas proteínas de origen animal se pliegan formando una hélice alfa (α-hélice) gracias a las interacciones puente de hidrógeno (Fuerzas intermoleculares) entre los aa. Otras proteínas, como la seda, forman una estructura que se conoce como hoja beta plegada. En algunas proteínas pueden coexistir ambas estructuras en diferentes regiones de la cadena peptídica.
Figura 4: Representación de α-hélice (arriba) y hoja plegada (abajo).
Figura 5. Representación de la estructura de la hemoglobina A humana.
Nombre
abreviatura (3 letras)
Gly
Ala
Val
Leu
Ile
El segundo grupo contiene los aminoácidos que tienen cadenas laterales aromáticas.
Nombre
abreviatura (3 letras)
Phe
Tyr
Trp
El tercer grupo de aminoácidos está compuesto de la serina (Ser) y la treonina (Thr).
Nombre
abreviatura (3 letras)
Pro
El sexto grupo está constituido por aminoácidos ácidos que contienen dos grupos carboxílicos.
Nombre
abreviatura (3 letras)
Asp
Glu
Asn
Gln
El séptimo grupo se encuentra constituido por los aminoácidos básicos.
isoleucina
leucina
lisina
metionina
fenilalanina
treonina
triptófano
valina
Por la especificidad de las proteínas, puede afirmarse que: las características de los organismos están dadas por el tipo y cantidad de proteínas que se sintetizan.
Las proteínas determinan la forma y la estructura de las células y dirigen casi todos los procesos vitales. Las funciones de las proteínas son específicas de cada una de ellas y permiten a las células mantener su integridad, defenderse de agentes externos, reparar daños, controlar y regular funciones.
Las proteínas se encuentran formadas por unidades o monómeros llamadas aminoácidos, existen 20 aminoácidos, de acuerdo a la repetición y secuencia de los mismos, se forma una cadena de aminoácidos (estructura primaria) llamados péptidos.
La estructura primaria de una proteína describe la cantidad y conectividad de aa. Los aa se unen entre sí “cabeza-cola” mediante un enlace covalente llamado enlace peptídico (o unión amida), la idea es formar uniones C-N. La reacción entre 2 aa se denomina condensación (ver Figura 3). Al unirse 2 aa forman un dipéptido, si se unen 3 aa se obtiene un tripéptido y así sucesivamente.
Figura 3. Representación de la reacción de condensación de 2 aa y formación del enlace peptídico (R1 y R2 pueden ser iguales o diferentes).
La estructura secundaria describe el modo en que una cadena peptídica se pliega o enrolla en el espacio. Muchas proteínas de origen animal se pliegan formando una hélice alfa (α-hélice) gracias a las interacciones puente de hidrógeno (Fuerzas intermoleculares) entre los aa. Otras proteínas, como la seda, forman una estructura que se conoce como hoja beta plegada. En algunas proteínas pueden coexistir ambas estructuras en diferentes regiones de la cadena peptídica.
La combinación de poderosas técnicas de análisis (difracción de rayos X, resonancia magnética nuclear y microscopía electrónica), simulación computacional y experimentos de dinámica molecular permite obtener imágenes de las macromoléculas. En el portal Protein Data Bank se encuentra almacenada esta valiosa información estructural (ver Figura 4).
Si disponen de conexión a Internet, accedan al portal Protein Data Bank, escriban el nombre de una proteína y busquen alguna imagen estructural relacionada con ella (el nombre debe ser tipiado en inglés y para eso pueden emplear el traductor).
Figura 4: Representación de α-hélice (arriba) y hoja plegada (abajo).
La estructura terciaria describe la forma en que la α-hélice, la hoja plegada u otra región de una proteína se organiza debido a interacciones entre algunos aa, por ejemplo, los puentes disulfuro (–S-S-) entre aa que contienen átomos de S (cisteína y metionina). La forma globular de algunas proteínas, como la hemoglobina responsable del transporte de O2, y otras sustancias como el óxido nítrico NO (un neurotransmisor) son ejemplos de estructura terciaria (ver Figura 5).
Figura 5. Representación de la estructura de la hemoglobina A humana.
La estructura cuaternaria describe el arreglo espacial de las cadenas peptídicas de las proteínas que están formadas por más de una unidad peptídica. Por ejemplo, la hemoglobina que se muestra en la Figura 5, está formada por 4 unidades peptídicas.
Aminoácidos
En el primer grupo, cada aminoácido contiene una cadena lateral alifática (una cadena hidrocarbonada no aromática).
Aminoácidos alifáticos
Nombre
|
abreviatura (3 letras)
|
Gly
| |
Ala
| |
Val
| |
Leu
| |
Ile
|
El segundo grupo contiene los aminoácidos que tienen cadenas laterales aromáticas.
Aminoácidos aromáticos
Nombre
|
abreviatura (3 letras)
|
Phe
| |
Tyr
| |
Trp
|
El tercer grupo de aminoácidos está compuesto de la serina (Ser) y la treonina (Thr).
Hidroxiaminoácidos
El cuarto grupo lo forman los aminoácidos que contienen azufre.
Tioaminoácidos
El quinto grupo está constituido únicamente por la prolina que es una amina secundaria.
Aminas secundarias
Nombre
|
abreviatura (3 letras)
|
Pro
|
El sexto grupo está constituido por aminoácidos ácidos que contienen dos grupos carboxílicos.
Aminoácidos dicarboxílicos
Nombre
|
abreviatura (3 letras)
|
Asp
| |
Glu
| |
Asn
| |
Gln
|
El séptimo grupo se encuentra constituido por los aminoácidos básicos.
Aminoácidos dibásicos
Aminoácidos esenciales
En la naturaleza no se encuentran ampliamente distribuidos los aminoácidos libres, pero que son los principales componentes de las proteínas. Para que nuestro cuerpo pueda sintetizar proteínas humanas, nuestra dieta debe proporcionar las proteínas animales y vegetales necesarias. Estas proteínas se hidrolizan (se divide la molécula) durante la digestión y se reesamblan para formar proteínas humanas.
Los aminoácidos se clasifican como esenciales y no esenciales en la dieta humana; son aminoácidos esenciales aquellos que se requieren en la dieta ya que no se pueden biosintetizar. Los ocho aminoácidos esenciales son:
isoleucina
|
leucina
|
lisina
|
metionina
|
fenilalanina
|
treonina
|
triptófano
|
valina
|
Por la especificidad de las proteínas, puede afirmarse que: las características de los organismos están dadas por el tipo y cantidad de proteínas que se sintetizan.
Si alguna proteína cambia su secuencia de aminoácidos o se produce escasamente, el resultado puede ser una característica diferente, una enfermedad, una enfermedad crónica con severas consecuencias o la muerte.
Por ejemplo, si la hemoglobina, proteína transportadora de oxígeno, que se encuentra en el interior de cada glóbulo rojo, es escasa o es diferente, consecuencia puede ser una anemia crónica o una enfermedad llamada anemia falciforme.
Si no se produce suficiente cantidad de melanina el color de la piel será claro, si no se fabrica melanina estamos frente a un albino.
Si no se fabrica en el páncreas la suficiente insulina la persona es diabética y la glucosa en sangre subirá hasta niveles de toxicidad capaz de matar células, entre ella neuronas.
Un déficit de proteasa, que es un enzima (proteína) que digiere al gluten para facilitar su absorción, es la causa más común de la celiaquía.
El orden en que se ubican los aminoácidos para formar una cadena que originará una proteína, y la cantidad de esta, así como su ubicación espacial, se encuentra codificado en el ADN.
Actividades para la experimentación
Deberás llevar el material necesario por grupo.
Deberás llevar el material necesario por grupo.
1
1. Este ejercicio los ayudará a comprender el concepto de estructura primaria de un péptido, polipéptido o proteína: Entendemos por estructura primaria la descripción de la secuencia de aa.
1. Este ejercicio los ayudará a comprender el concepto de estructura primaria de un péptido, polipéptido o proteína: Entendemos por estructura primaria la descripción de la secuencia de aa.
Supongan que disponen de 4 ganchitos para papel de diferente color: uno verde, uno azul, uno rojo y otro lila. ¿Cuántas combinaciones se pueden obtener al ensamblarlos entre sí linealmente?
a) Trabajen en pequeños grupos y armen todas las combinaciones posibles empleando ganchitos para papel o perlas para collares. Registren el resultado empleando la cámara digital de sus equipos portátiles.
b) Verifiquen que el número de posibles combinaciones de péptidos a obtener es: 4 x 3 x 2 x 1 = 24.
c) Si se partiera de 6 ganchitos de colores diferentes, ¿cuántas secuencias se obtendrían? Razonen de manera análoga al caso anterior.
d) Apliquen la misma estrategia para escribir, empleando el programa Writer de sus equipos portátiles, todos los péptidos que se pueden obtener combinando 4 aa diferentes. Por ejemplo: Ala (alanina), Lys (lisina), Val (valina) y Met (metionina). El número de péptidos posibles debe ser igual al número de combinaciones que se obtuvieron con los ganchitos de colores.
2. El paso siguiente es visualizar la estructura 3D de un péptido. Para eso, empleen el programa Chem Sketch o el Avogadro.
a) Representen el aa alanina y visualicen su estructura 3D. Utilicen diferentes representaciones (bolas y palitos, puntos, etc.) y roten la molécula en el espacio.
b) Ensamblen 2 aa alanina formando un dipéptido. Luego, agreguen uno más y un cuarto. Visualicen la estructura 3D del tetrapéptido obtenido. Identifiquen las uniones peptídicas.
c) Repitan la actividad ensamblando diferentes aa. Les sugerimos emplear los mismos aa que se usaron previamente. Cada alumno puede armar un péptido diferente.
2
La pérdida de la estructura (primaria, secundaria, terciaria o cuaternaria) de una proteína se conoce como desnaturalización. En algunos casos, este proceso puede ser reversible, como ocurre en la formación de rulos en el cabello o el alisamiento del mismo (este efecto se relaciona con la formación o ruptura de puentes –S-S- en la α-hélice de la queratina). Pero cuando se hace un huevo frito, por ejemplo, las proteínas de la clara del huevo se desnaturalizan y este cambio es irreversible.
La pérdida de la estructura (primaria, secundaria, terciaria o cuaternaria) de una proteína se conoce como desnaturalización. En algunos casos, este proceso puede ser reversible, como ocurre en la formación de rulos en el cabello o el alisamiento del mismo (este efecto se relaciona con la formación o ruptura de puentes –S-S- en la α-hélice de la queratina). Pero cuando se hace un huevo frito, por ejemplo, las proteínas de la clara del huevo se desnaturalizan y este cambio es irreversible.
La desnaturalización es provocada por diferentes factores, entre ellos: el cambio de pH, la temperatura, la polaridad del solvente, la presencia de iones en el sistema (fuerza iónica). La desnaturalización afecta marcadamente la funcionalidad de las proteínas. Por ejemplo, las enzimas suelen perder su capacidad catalítica (ver secuencia didáctica Catalizadores y conservantes) al ser calentadas por encima de cierta temperatura.
· Visualizar el proceso de desnaturalización de la albúmina de la clara de huevo.
a) Filmen el experimento con las cámaras de sus equipos portátiles.
b) Redacten un guión que explique los pasos y las observaciones y acompañe al material que filmaron.
Materiales
Huevo de gallina crudo.
Etanol o alcohol de uso medicinal (96% v/v).
Plato o bandeja de plástico.
Vaso.
Cuchara.
Procedimiento
1. Rompan el huevo y separen la clara de la yema. Viertan la clara en el plato o bandeja. La cáscara y la yema se pueden desechar en el vaso.
2. Agreguen 2 o 3 cucharadas de alcohol sobre la clara.
3. Observen los cambios que se producen. Comparen con el aspecto de un huevo frito.
Actividad 2
Realizar en Word y enviar a viviairaldo09@gmail.com
Orientadores de análisis
1.- Comente las propiedades de los aminoácidos. ¿Qué son y cómo se forman los péptidos?
6. La configuración  o de lámina plegada de una proteína, se refiere a:
o de lámina plegada de una proteína, se refiere a:
8) Cuando una proteína se desnaturaliza,
9) La especificidad de las proteínas es consecuencia de:
http://www.elmundo.es/especiales/2003/02/salud/genetica/descifrar_la_vida.html
Realizar las actividades
A. Análisis de recortes de seis artículos seleccionados.
Cada uno posee un link para poder leerlo en forma completa.ARTICULO 1
El gen fumador - El gen "adictivo"
Probar el cigarrillo es parte de un rito común entre muchos adolescentes, pero disfrutarlo o no depende de la genética, sugieren algunos investigadores. Genes determinan que a algunos nos "enganche" más el cigarrillo.
…”Científicos de la Universidad de Míchigan identificaron una mutación genética frecuente en personas que sintieron una fuerte sensación agradable con su primer cigarrillo. La decisión de fumar por primera vez y continuar con el vicio no depende únicamente de la influencia de sus genes, pero si forma parte de una mezcla de factores como los ambientales y la presión social. El gen en cuestión, el CHRNA5 fue identificado por otros estudios vinculados a la adicción a la nicotina, y se cree que podría incrementar la posibilidad de desarrollar cáncer de pulmón”….
ARTICULO 2
SALUD Y BIENESTAR
- Conozcamos Nuestro Organismo La Estatura es Hereditaria
…”La talla de cada persona está determinada genéticamente y establecida desde su nacimiento, y por tal motivo es posible predecir la estatura final de ésta”. …”Lo que sucede durante los 20 primeros años de crecimiento está predeterminado en su mayor parte antes del nacimiento, pues la talla final depende fundamentalmente de factores genéticos. No se conoce con seguridad el número de genes que intervienen, y aún se sabe menos sobre cómo se combinan entre sí cuando se engendra una nueva vida. Lo que sí es cierto es que la talla de una persona se hereda. Pero el crecimiento puede verse afectado también por factores externos como la alimentación o ambiente medio”...
Copyright © 2013 El Aviso Magazine. All Rights Reserved. Designed by JoomShaper Scroll to Top Joomla15 Appliance - Powered by TurnKey Linux
ARTICULO 3
….”Llevó a cabo estudios moleculares detallados del material genético -la secuencia de ADN- de los cromosomas X de 40 parejas de hermanos homosexuales, con el fin de investigar los marcadores genéticos…. El científico comprobó que en 33 de los casos ambos hermanos habían heredado los mismos marcadores genéticos de una zona del cromosoma X conocida como Xq28”…
….”Aunque Hammer no descubrió un gen de la homosexualidad masculina, sí encontró pruebas convincentes de que esa región influye en la orientación sexual de algunos varones”….
ARTICULO 4
…”Un reciente estudio llevado a cabo en Suecia por el Instituto Karolinska, revela que homosexual se nace. A semejante conclusión llegaron a través de una medición que consistió en analizar áreas del cerebro de 90 personas, mitad hombres y mujeres heterosexuales y la otra mitad gays y lesbianas, a través de imágenes obtenidas por resonancia magnética para medir el volumen del cerebro, descubriendo que las medidas de los gays son similares a los de las mujeres y viceversa, que los de las lesbianas son similares a los de los varones”
ARTICULO 5
“Un nobel de medicina dice que la estupidez se puede curar”
…..”Entre las controvertidas declaraciones que se conocieron ayer en Londres, Watson, de 75 años, sostiene que "las personas estúpidas o con un coeficiente intelectual bajo que no tienen un trastorno mental diagnosticado padecen un desorden que se transmite en forma hereditaria a través de los genes, como ocurre con enfermedades como la fibrosis cística o la hemofilia".
El prestigioso profesor, defensor a ultranza de la idea de usar la ingeniería genética para mejorar la raza humana, aseguró: "Si eres estúpido, yo a eso lo llamaría enfermedad". Y consideró que es un "error" asociar la lentitud en el aprendizaje a una situación de pobreza o a problemas familiares, ya que "es más probable que exista una causa genética que puede y debe ser corregida"… [http://edant.clarin.com/diario/2003/03/01/s-04401.htm.]
Científicos suecos descubren un gen vinculado a la infidelidad masculina
De ahí que los hombres dotados de esta variante del gen sean peligrosos para una relación estable -algunos y algunas ya lo sabían por experiencia-, pero ahora lo ha constatado el estudio de los científicos suecos.
"Cariño, la culpa la tiene el alelo". Y es que el alelo 334 se encarga del receptor de la arginina vasopresina, que es una hormona básica y que está presente en el cerebro de la mayoría de los mamíferos, según esta investigación.
El descubrimiento radica en que "es la primera vez que se asocia la variante de un gen específico con la manera en que los hombres se comprometen con sus parejas"
1.- Comente las propiedades de los aminoácidos. ¿Qué son y cómo se forman los péptidos?
2.- Describa las características de los niveles de organización estructural de las proteínas.
3.- Explique a qué se refiere la especificidad de las proteínas y por qué puede plantear problemas en los trasplantes de órganos.
4.- Funciones de las proteínas. Cite ejemplos de proteínas (nombres específicos, por ejemplo: hemoglobina) y funciones concretas que desempeñen en el organismo.
5. Las proteínas son macromoléculas biológicas constituidas básicamente por:
C, H, O, P.
C, H, O, N.
C, H, O, Fe
6. La configuración  o de lámina plegada de una proteína, se refiere a:
o de lámina plegada de una proteína, se refiere a:
Su estructura primaria.
Su estructura secundaria.
Su estructura terciaria.
8) Cuando una proteína se desnaturaliza,
Se destruye
Se destruye su estructura terciaria
9) La especificidad de las proteínas es consecuencia de:
La capacidad de cada ser vivo para fabricar sus propias proteínas.
La capacidad de cada ser vivo para rechazar sus propias proteínas.
Ambas respuestas son correctas.
10) El colágeno es una proteína con función:
Estructural.
Enzimática.
Hormonal.
http://www.elmundo.es/especiales/2003/02/salud/genetica/descifrar_la_vida.html
Realizar las actividades
Realizar las actividades
A. Análisis de recortes de seis artículos seleccionados.
Cada uno posee un link para poder leerlo en forma completa.ARTICULO 1
El gen fumador - El gen "adictivo"
|
Probar el cigarrillo es parte de un rito común entre muchos adolescentes, pero disfrutarlo o no depende de la genética, sugieren algunos investigadores. Genes determinan que a algunos nos "enganche" más el cigarrillo.
|
…”Científicos de la Universidad de Míchigan identificaron una mutación genética frecuente en personas que sintieron una fuerte sensación agradable con su primer cigarrillo. La decisión de fumar por primera vez y continuar con el vicio no depende únicamente de la influencia de sus genes, pero si forma parte de una mezcla de factores como los ambientales y la presión social. El gen en cuestión, el CHRNA5 fue identificado por otros estudios vinculados a la adicción a la nicotina, y se cree que podría incrementar la posibilidad de desarrollar cáncer de pulmón”….
|
ARTICULO 2
SALUD Y BIENESTAR
|
- Conozcamos Nuestro Organismo La Estatura es Hereditaria
|
…”La talla de cada persona está determinada genéticamente y establecida desde su nacimiento, y por tal motivo es posible predecir la estatura final de ésta”. …”Lo que sucede durante los 20 primeros años de crecimiento está predeterminado en su mayor parte antes del nacimiento, pues la talla final depende fundamentalmente de factores genéticos. No se conoce con seguridad el número de genes que intervienen, y aún se sabe menos sobre cómo se combinan entre sí cuando se engendra una nueva vida. Lo que sí es cierto es que la talla de una persona se hereda. Pero el crecimiento puede verse afectado también por factores externos como la alimentación o ambiente medio”...
|
Copyright © 2013 El Aviso Magazine. All Rights Reserved. Designed by JoomShaper Scroll to Top Joomla15 Appliance - Powered by TurnKey Linux
|
ARTICULO 3
EL 'GEN DE LA HOMOSEXUALIDAD' VUELVE A DEBATE
…”Las últimas investigaciones de Hammer, que aparentemente confirman la existencia de un componente genético, de la homosexualidad, han vuelto a atizar la polémica sobre el carácter genético de los aspectos más sensibles del comportamiento humano” ….
….”Llevó a cabo estudios moleculares detallados del material genético -la secuencia de ADN- de los cromosomas X de 40 parejas de hermanos homosexuales, con el fin de investigar los marcadores genéticos…. El científico comprobó que en 33 de los casos ambos hermanos habían heredado los mismos marcadores genéticos de una zona del cromosoma X conocida como Xq28”…
….”Aunque Hammer no descubrió un gen de la homosexualidad masculina, sí encontró pruebas convincentes de que esa región influye en la orientación sexual de algunos varones”….
….”Llevó a cabo estudios moleculares detallados del material genético -la secuencia de ADN- de los cromosomas X de 40 parejas de hermanos homosexuales, con el fin de investigar los marcadores genéticos…. El científico comprobó que en 33 de los casos ambos hermanos habían heredado los mismos marcadores genéticos de una zona del cromosoma X conocida como Xq28”…
….”Aunque Hammer no descubrió un gen de la homosexualidad masculina, sí encontró pruebas convincentes de que esa región influye en la orientación sexual de algunos varones”….
ARTICULO 4
UN NUEVO ESTUDIO REVELA QUE GAY SE NACE
http://www.periodismoenlared.com/estudio-revela-nace
…”Un reciente estudio llevado a cabo en Suecia por el Instituto Karolinska, revela que homosexual se nace. A semejante conclusión llegaron a través de una medición que consistió en analizar áreas del cerebro de 90 personas, mitad hombres y mujeres heterosexuales y la otra mitad gays y lesbianas, a través de imágenes obtenidas por resonancia magnética para medir el volumen del cerebro, descubriendo que las medidas de los gays son similares a los de las mujeres y viceversa, que los de las lesbianas son similares a los de los varones”
…”Un reciente estudio llevado a cabo en Suecia por el Instituto Karolinska, revela que homosexual se nace. A semejante conclusión llegaron a través de una medición que consistió en analizar áreas del cerebro de 90 personas, mitad hombres y mujeres heterosexuales y la otra mitad gays y lesbianas, a través de imágenes obtenidas por resonancia magnética para medir el volumen del cerebro, descubriendo que las medidas de los gays son similares a los de las mujeres y viceversa, que los de las lesbianas son similares a los de los varones”
ARTICULO 5
“Un nobel de medicina dice que la estupidez se puede curar”
http://edant.clarin.com/diario/2003/03/01/s-04401.htm
…..”Entre las controvertidas declaraciones que se conocieron ayer en Londres, Watson, de 75 años, sostiene que "las personas estúpidas o con un coeficiente intelectual bajo que no tienen un trastorno mental diagnosticado padecen un desorden que se transmite en forma hereditaria a través de los genes, como ocurre con enfermedades como la fibrosis cística o la hemofilia".
El prestigioso profesor, defensor a ultranza de la idea de usar la ingeniería genética para mejorar la raza humana, aseguró: "Si eres estúpido, yo a eso lo llamaría enfermedad". Y consideró que es un "error" asociar la lentitud en el aprendizaje a una situación de pobreza o a problemas familiares, ya que "es más probable que exista una causa genética que puede y debe ser corregida"… [http://edant.clarin.com/diario/2003/03/01/s-04401.htm.]
…..”Entre las controvertidas declaraciones que se conocieron ayer en Londres, Watson, de 75 años, sostiene que "las personas estúpidas o con un coeficiente intelectual bajo que no tienen un trastorno mental diagnosticado padecen un desorden que se transmite en forma hereditaria a través de los genes, como ocurre con enfermedades como la fibrosis cística o la hemofilia".
El prestigioso profesor, defensor a ultranza de la idea de usar la ingeniería genética para mejorar la raza humana, aseguró: "Si eres estúpido, yo a eso lo llamaría enfermedad". Y consideró que es un "error" asociar la lentitud en el aprendizaje a una situación de pobreza o a problemas familiares, ya que "es más probable que exista una causa genética que puede y debe ser corregida"… [http://edant.clarin.com/diario/2003/03/01/s-04401.htm.]
ARTICULO 6
DOS DE CADA CINCO HOMBRES TIENEN ESTA VARIANTE
Científicos suecos descubren un gen vinculado a la infidelidad masculina
Científicos suecos descubren un gen vinculado a la infidelidad masculina
ESTOCOLMO.- Ahora parece ser que la culpa de la infidelidad de los hombres la va a tener un gen, el alelo 334, que gestiona la vasopresina, una hormona que se produce naturalmente, por ejemplo, con los orgasmos, según un estudio del Instituto Karolinska de Estocolmo.
De ahí que los hombres dotados de esta variante del gen sean peligrosos para una relación estable -algunos y algunas ya lo sabían por experiencia-, pero ahora lo ha constatado el estudio de los científicos suecos.
"Cariño, la culpa la tiene el alelo". Y es que el alelo 334 se encarga del receptor de la arginina vasopresina, que es una hormona básica y que está presente en el cerebro de la mayoría de los mamíferos, según esta investigación.
El descubrimiento radica en que "es la primera vez que se asocia la variante de un gen específico con la manera en que los hombres se comprometen con sus parejas"
De ahí que los hombres dotados de esta variante del gen sean peligrosos para una relación estable -algunos y algunas ya lo sabían por experiencia-, pero ahora lo ha constatado el estudio de los científicos suecos.
"Cariño, la culpa la tiene el alelo". Y es que el alelo 334 se encarga del receptor de la arginina vasopresina, que es una hormona básica y que está presente en el cerebro de la mayoría de los mamíferos, según esta investigación.
El descubrimiento radica en que "es la primera vez que se asocia la variante de un gen específico con la manera en que los hombres se comprometen con sus parejas"
Actividad 1
Realizar en Word y enviar a viviairaldo09@gmail.com
¿Existe el determinismo genético? Orientadores de análisis
1.- La característica / comportamiento / desempeño presentado es el resultado de (macar con una cruz):
( ) a.- La expresión de los genes
( ) b.- Condiciones ambientales diversas.
( ) c. La interacción genes-ambiente.
2.- ¿Qué pruebas o evidencias encuentra para justificar su elección en el ítem 1?
Expresión de los genes
Condiciones ambientales diversas
Interacción genes- ambiente
Pruebas o evidencias
Hipótesis o explicaciones
B. Argumentando conclusiones
Elaborar una conclusión sobre la pregunta inicial, argumentando la misma con los conceptos extraídos del análisis de los artículos y el ensayo que sigue.
1.- La característica / comportamiento / desempeño presentado es el resultado de (macar con una cruz):
( ) a.- La expresión de los genes
( ) b.- Condiciones ambientales diversas.
( ) c. La interacción genes-ambiente.
2.- ¿Qué pruebas o evidencias encuentra para justificar su elección en el ítem 1?
( ) a.- La expresión de los genes
( ) b.- Condiciones ambientales diversas.
( ) c. La interacción genes-ambiente.
2.- ¿Qué pruebas o evidencias encuentra para justificar su elección en el ítem 1?
3.- ¿Qué hipótesis o explicaciones se brindan en cada artículo?
4- Para la puesta en común: cada grupo completará el cuadro, de tal manera que el registro que favorezca posteriormente un análisis comparativo, el mismo puede organizarse utilizando las netbook o pueden registrarse en afiches elaborados por cada equipo.
5- Exponer y explicar en el momento del plenario.
Expresión de los genes
|
Condiciones ambientales diversas
|
Interacción genes- ambiente
| |
Pruebas o evidencias
| |||
Hipótesis o explicaciones
|
B. Argumentando conclusiones
Elaborar una conclusión sobre la pregunta inicial, argumentando la misma con los conceptos extraídos del análisis de los artículos y el ensayo que sigue.
Compuestos químicos
Óxidos: Son compuestos binarios formados por
combinación del oxígeno en su número de oxidación –2, con otro elemento, que
llamaremos E, actuando con valencia (n) positiva. (La valencia de un elemento
es el número de oxidación, sin signo). Su fórmula general es:
Existen cuatro clases de óxidos:
Cuando hablamos de
los óxidos dijimos que había cuatro clases y una de ellas, los óxidos básico u
óxidos metálicos, producía al mezclarse con agua, los hidróxidos.
Oxoácidos: Son compuestos ternarios, formados por
la combinación de tres elementos distintos, Hidrógeno, Oxígeno y otro elemento,
que por ahora llamaremos E, y que en la mayoría de los casos es no metálico
(más adelante cuando estudiemos los óxidos anfóteros veremos algunos casos en
los que E es un metal). La fórmula general de los oxoácidos es: HaEbOc
H3PO4 Ácido Ortofosfórico
AlH3
HI / H2S
2 NaOH (ac) H2SO4 (ac) Na2SO4 (ac) + 2 H2O (l)
En los ejercicios
anteriores, habrás notado que el oxígeno se combinaba con diferentes tipos de
elementos. Esto determina el tipo de óxido formado, y otras particularidades,
como su comportamiento frente al agua y el tipo de compuesto que forman en este
caso.
Es muy importante que
recuerdes:
Solo se pueden
modificar los coeficientes, pero nunca los subíndices. Si cambio un
coeficiente, solo varía la “cantidad” de veces que “ese” compuesto está
presente en la reacción. Pero al cambiar un subíndice, cambia la “identidad”
del compuesto.
Las letras entre
paréntesis a la derecha de cada compuesto indican su estado de agregación, es
decir, si son sólidos (s), líquidos (l), gaseosos (g) o acuosos (ac). Siempre
acompañan a los compuestos químicos en una reacción y a veces, permiten
diferenciar entre dos compuestos con la misma fórmula y distintas
características (hidruros e hidrácidos).
Aclaración: si bien
podemos plantear una reacción de obtención para todos los compuestos, no
necesariamente esta sea la vía por la que se forman en la naturaleza,
simplemente la planteamos con fines didácticos, para que te sea más simple
entender el proceso, así como también, que puedas practicar un poco más.
Ahora estás
nuevamente en condiciones de realizar solo algunos ejercicios.
EJERCITACIÓN
UNIONES QUÍMICAS
1-
Representar las estructuras de Lewis de
las siguientes sustancias iónicas:
a) LiF b) BaBr2 c) MgS d)
Na3P e) AlCl3
2-
Representar las estructuras de Lewis y las fórmulas mínimas
de las sustancias formadas por:
a) 19K
y 17Cl b) 20
Ca y 8 O c) 3Li y 16S d) 13Al
y 9F e) 11Na
y 7 N
3-
Escribir las estructuras de Lewis y las
fórmulas mínimas de las siguientes sustancias:
a)
Bromuro de hierro ( III)
7-
Para
el elemento de Z = 12, responder:
a)
¿Tiene
tendencia a formar cationes o aniones?
8-
El
elemento O (oxígeno) pertenece al 2º período y grupo 16 de la tabla periódica.
El elemento X tiene número atómico 37.
a)
Escribir
la configuración electrónica para cada elemento.
9-
Dados
los elementos que figuran en el siguiente esquema de la tabla periódica
m
f
i
a
b
h
g
n
e
c
d
l
a)
¿
Qué tipo de unión puede formar el elemento d
con el elemento e?
Sustancias con Enlace Iónico
Puntos de
ebullición y de fusión.
Sustancia
Punto de fusión en °C
NaCl
801
BaCl2
963
LiF
845
CaF2
1360
Dureza.
Escala de Mohs
valor
Talco
1
Yeso
2
Calcita
3
Fluorita
4
Apatito
5
Ortosa
6
cuarzo
7
Topacio
8
Corindón
9
diamante
10
Solubilidad.
Conductividad.
Sustancias con Enlace Covalente
Estado de
agregación a temperatura y presión ambiente.
Punto de fusión y
de ebullición.
Punto de fusión y
de ebullición.
Conductividad.
Sustancias con Enlace Metálico
Punto de fusión.
Puntos de fusión de algunos metales (ºC)
Li (180)
Be (1280)
.
.
.
.
Na (98)
Mg (650)
Al (660)
Ti (1800)
Fe (1530)
Cu (1083)
K (64)
Ca (838)
Ga (29,7)
Zr (1700)
Co(1480)
Ag (961)
Rb (39)
Sr (770)
.
.
.
Sn (232)
Cs (29)
Ba (725)
.
.
.
Pb (328)
Conductividad eléctrica.
Conductividad térmica.
Brillo.
Solubilidad.
10- Ordenar
las siguientes sustancias según sus puntos de fusión crecientes:
AlBr3 ;
LiBr y CaBr2
11- Indicar
cuál de las siguientes características pertenecen a las sustancias iónicas:
Na2S ;
Hg ; Li2O ; GaN ; OF2
17- Dar una
explicación a los puntos de ebullición ( en º C) de los siguientes fluoruros:
NaF ( 988) ; MgF2 ( 1266 ) ; AlF3 (
1291)
UNIONES QUÍMICAS
1-
Representar las estructuras de Lewis de
las siguientes sustancias iónicas:
a) LiF b) BaBr2 c) MgS d)
Na3P e) AlCl3
f) PbS2 g) K2O h) Ca3N2 i)
SnBr4 j) Ga2O3
2-
Representar las estructuras de Lewis y las fórmulas mínimas
de las sustancias formadas por:
a) 19K
y 17Cl b) 20
Ca y 8 O c) 3Li y 16S d) 13Al
y 9F e) 11Na
y 7 N
3-
Escribir las estructuras de Lewis y las
fórmulas mínimas de las siguientes sustancias:
a)
Bromuro de hierro ( III)
b)
Seleniuro de sodio
c)
Sulfuro de aluminio
d)
Óxido de hierro (III)
e)
Nitruro de hierro (II)
f)
Nitruro de cobalto (III)
g)
Cloruro de plomo (IV)
h)
Fosfuro de calcio
i)
Arseniuro de galio
j)
Yoduro de niquel (III)
k)
Fosfuro de oro (I)
l)
Óxido de oro (III)
m
f
i
a
b
h
g
n
e
c
d
l
Sustancias con Enlace Iónico
Puntos de
ebullición y de fusión.
Las sustancias
que presentan enlaces iónicos son sólidas a temperatura y presión ambiente
pues sus puntos de fusión y ebullición son altos debido a que al encontrarse
los iones fuertemente atraídos (como nos referimos en interacciones entre
partículas) se requiere mucha energía para poder separarlos y que puedan
cambiar de estado. Cuanto mayor es la carga o menor es la distancia entre los
iones, más elevados son los puntos de fusión y de ebullición.
Sustancia
|
Punto de fusión en °C
|
NaCl
|
801
|
BaCl2
|
963
|
LiF
|
845
|
CaF2
|
1360
|
Dureza.
La dureza es la
resistencia que ofrecen los sólidos a ser rayados. La propia estructura
ordenada de los sólidos iónicos, explica su dureza, ya que no hay lugar hacia
donde se desplacen los iones bajo presión. Para rayar un cristal es necesario
romper los enlaces entre iones (op.cit. en interacciones entre partículas).
La dureza varía desde 1 a 9 en la escala de Mohs.
Escala de Mohs
|
valor
|
Talco
|
1
|
Yeso
|
2
|
Calcita
|
3
|
Fluorita
|
4
|
Apatito
|
5
|
Ortosa
|
6
|
cuarzo
|
7
|
Topacio
|
8
|
Corindón
|
9
|
diamante
|
10
|
Solubilidad.
Los disolventes
polares hacen disminuir las fuerzas atractivas al interponerse las moléculas
del disolvente entre los iones. Cada ion se rodea de moléculas de disolvente
(solvatación). La solubilidad disminuye si aumenta la carga de los iones. Así
las sustancias formadas por metales del grupo II A (alcalinos térreos) son
menos solubles que las formadas por metales del grupo I A (alcalinos)
Conductividad.
Las que presentan
enlace iónico tienen sus electrones muy bien localizados, es decir que los
iones en los cristales carecen de movilidad; sin embargo cuando están
fundidos o disueltos en soluciones acuosas, como los iones se encuentran
libres, es decir adquieren movilidad, por lo cual conducen la corriente
eléctrica y el calor.
Medidor de
conductividad video
Sustancias con Enlace Covalente
Estado de
agregación a temperatura y presión ambiente.
Los compuestos
covalentes pueden existir en los tres estados debido a las atracciones entre
moléculas.
Punto de fusión y
de ebullición.
En general tienen
bajos puntos de ebullición y de fusión que dependen del tipo de atracción que
tengan las moléculas.
Punto de fusión y
de ebullición.
En general tienen
bajos puntos de ebullición y de fusión que dependen del tipo de atracción que
tengan las moléculas.
Conductividad.
En general, son
malos conductores de la electricidad y del calor, justamente porque en
solución o en estado de fusión no poseen partículas con cargas libres (a
diferencia de las sustancias con enlace iónico), que permitan que se cumpla
esta propiedad.
Sustancias con Enlace Metálico
|
||||||||||||||||||||||||||||||||
Punto de fusión.
Como se sabe para fundir un metal se le debe proporcionar calor para
que el movimiento de vibración de los átomos se haga más intenso hasta que
terminan por separarse del sólido. Naturalmente cuanto más fuerte son los
enlaces entre los átomos, mayor será la energía calorífica necesaria para
separarlos y, por ello, más elevado será el punto de fusión. En los
metales, los puntos de fusión abarcan un espectro amplio: desde valores
relativamente bajos como el del cesio, a muy elevados como el del platino.
Existe una cierta tendencia de los puntos de fusión a aumentar de izquierda
a derecha, en el mismo período, y disminuir conforme aumenta el número
atómico en el mismo grupo en la tabla periódica
|
||||||||||||||||||||||||||||||||
Puntos de fusión de algunos metales (ºC)
|
||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||
Conductividad eléctrica.
Los metales conducen fácilmente la corriente eléctrica, en estado
sólido y fundidos, ya que los electrones se desplazan con facilidad, por
atracción o repulsión entre cargas de igualo diferente signo, bajo la
acción de un potencial eléctrico.
|
||||||||||||||||||||||||||||||||
Conductividad térmica.
El movimiento de las partículas genera choques, un aumento en la
temperatura influye en la energía cinética de las partículas aumentando así
mismo la velocidad de los electrones y, por lo tanto, la transmisión de la
energía calórica generada.
|
||||||||||||||||||||||||||||||||
Brillo.
La incidencia de la luz sobre la superficie de los metales hace que
los electrones vibren, por lo que se originan ondas electromagnéticas de la
misma frecuencia que la luz incidente.
|
||||||||||||||||||||||||||||||||
Solubilidad.
Son insolubles en agua o en otros solventes no polares. Sí son
solubles en otros metales (aleaciones o solución sólido en sólido). Algunos
metales, como el sodio, reaccionan en forma violenta cuando se ponen en
contacto con el agua.
|
||||||||||||||||||||||||||||||||
Recomiendo que miren este video para comprender todo sobre la tabla periódica.
Definir qué significa PERIÓDICA, y ejemplificar de diferentes maneras.
QUÍMICA GENERALTRABAJO PRÁCTICOS Y RECURSOSOrganizador de la tarea:Actividad de revisión:Recurso: apuntes de clases anteriores.PARA CARACTERIZAR UN CUERPO MATERIAL NOMBRAMOS SUS PROPIEDADES GENERALES:
ü Ocupa un lugar, por lo que se dice que tiene EXTENSIÓN.
ü Todos los cuerpos materiales tienden a permanecer en el estado que presentan, de movilidad o reposo/posición, es decir presenta INERCIA.
ü Dos cuerpos no pueden ocupar el mismo espacio al mismo tiempo ya que la materia es IMPENETRABLE.
ü Como consecuencia de la interacción con fuerzas los cuerpos pueden cambiar de posición es decir poseen MOVILIDAD.
1. Reconocer cada una a través de la realización de alguna de las experiencias que figuran en la última hoja.
2. Demostrar empíricamente 2 dos de las experiencias.
Y PROPIEDADES ESPECÍFICAS, PROPIAS DE CADA SUSTANCIA:
3. COLOCA CADA PROPIEDAD EN LA COLUMNA QUE CORRESPONDE:
PESO – CANTIDAD DE MATERIA atraída por la gravedad; COLOR, AROMA, SABOR, TEXTURA, SONIDO: PROPIEDADES ORGANOLÉPTICAS (QUE SE PUEDEN PERCIBIR A TRAVÉS DE LOS SENTIDOS); PUNTO DE EBULLICIÓN; DENSIDAD: MASA/VOLUMEN; MASA – CANTIDAD DE MATERIA; LONGITUD; VOLUMEN; EVAPORACIÓN-SOLIDIFICACIÓN-FUSIÓN; VELOCIDAD; CANTIDAD DE ENERGÍA; CONDUCTOR O NO DEL CALOR Y LA ELECTRICIDAD; ESTADO DE AGREGACIÓN (SÓLIDO-LÍQUIDO-GASEOSO); SUPERFICIE.
ü Todos los cuerpos materiales tienden a permanecer en el estado que presentan, de movilidad o reposo/posición, es decir presenta INERCIA.
ü Como consecuencia de la interacción con fuerzas los cuerpos pueden cambiar de posición es decir poseen MOVILIDAD.
CANTIDAD - CUANTITATIVAS
|
CALIDAD – CUALITATIVAS
|
ESTAS PROPIEDADES DESCRIBEN CUÁNTO HAY DE MATERIA.
|
ESTAS PROPIEDADES DESCRIBEN CÓMO ES LA MATERIA
|
4. Identificar colocando: intensiva o extensiva, según corresponda:
Distancia de la Tierra al sol.
Color verde de la cúpula del Congreso Nacional.
Densidad del aluminio.
Brillo del metal.
Superficie de la franja de Gaza.
5. Relaciona y define los siguientes conceptos en una red conceptual cuyas flechas posean palabras nexos: elemento químico, átomo, número de protones; símbolo; materia; sustancia; simple; compuesta; mezclas; soluciones; puras; homogéneas, heterogéneas, tabla periódica.
Actividad de aplicación y comprensión
Recursos: Explicaciones de la clase actual, lápices de colores y texto 1
6. Colorear y completar la tabla periódica según corresponda:
Recursos: Explicaciones de la clase actual, lápices de colores y texto 1
A. Indicar el significado de números e inscripciones de cada casillero, utilizando como referencia el Carbono.
B. Los nombres y los símbolos tienen su origen e historia, realiza un resumen luego de la lectura del Texto 1
Analizando el orden de los elementos:
C. Define PERÍODOS (cortos, largos)
D. Define GRUPOS y pintar con celeste los grupos representativos (A) correspondiente a metales alcalinos, con azul los metales alcalinos térreos, con rojo los grupos representativos correspondiente a no metales, con naranja los metaloides, con verde los elementos de transición interna y dejar sin color a los Gases Nobles. Con resaltador los lantánidos y los actínidos y los dos elementos que le dan el nombre.
E. Colocar una G a los elementos gaseosos, una S a los sólidos y una L a los líquidos a temperatura ambiente y 1 atmósfera de presión atmosférica.
F. Colocar el nombre de cada uno de los grupos de la tabla periódica.
Actividad de investigación
Recursos: texto 2 y 3, programa CRONOS, aplicación PREZI o POWER POINT
G. Preparar en grupo la caracterización de cada uno de los grupos de la tabla periódica, acompañar la exposición con imágenes de los elementos, lugares donde abundan o se extraen habitualmente, reacciones con el oxígeno o con el agua, propiedades de conductibilidad de la electricidad o el calor, uso como recurso natural (industria farmacéutica, alimentaria, metalúrgica, bioingeniería, entre otras). Texto de referencia 2
H. Investigar cada dos personas (texto de referencia 3):
1. ¿Qué es la química?
2. ¿Cuál es el origen histórico de la química?
3. ¿Cuáles fueron los principales hitos que permitieron la construcción y completamiento de la tabla periódica? Construir una línea del tiempo. (CRONOS)
Texto 1: Procedencia de los nombres de algunos elementos químicos.
Nombres de elementos en honor a planetas y asteroides:
Mercurio, su nombre se debe al planeta del mismo nombre, pero su abreviatura es Hg. Dioscórides lo llamaba plata acuática (en griego hydrárgyros). hydra=agua, gyros= plata.
Uranio (U): del planeta Urano.
Neptunio (Np): del planeta Neptuno.
Plutonio (Pu): del planeta Plutón.
Cerio (Ce): por el asteroide Ceres, descubierto dos años antes. (¿Sabíais que el cerio metálico se encuentra principalmente en una aleación de hierro que se utiliza en las piedras de los encendedores?).
Titanio(Ti): de los Titanes, los primeros hijos de la Tierra según la mitología griega.
Uranio (U): del planeta Urano.
Neptunio (Np): del planeta Neptuno.
Plutonio (Pu): del planeta Plutón.
Cerio (Ce): por el asteroide Ceres, descubierto dos años antes. (¿Sabíais que el cerio metálico se encuentra principalmente en una aleación de hierro que se utiliza en las piedras de los encendedores?).
Titanio(Ti): de los Titanes, los primeros hijos de la Tierra según la mitología griega.
Nombres de lugares y similares:
Magnesio (Mg): de Magnesia, comarca de Tesalia (Grecia).
Scandio (Sc) Scandia, Escandinavia ( por cierto, Vanadio (V): Vanadis, diosa escandinava).
Cobre (Cu): cuprum, de la isla de Chipre.
Galio (Ga): de Gallia, Francia.
Germanio(Ge): de Germania, Alemania.
Selenio (Se):de Selene, la Luna.
Estroncio (Sr): Strontian, ciudad de Escocia.
Itrio (Y): de Ytterby, pueblo de Suecia.
Rutenio (Ru): del latín Ruthenia, Rusia.
Terbio (Tb): de Ytterby, pueblo de Suecia.
Europio (Eu): de Europa.
Holmio (Ho): del latín Holmia, Estocolmo.
Tulio (Tm): de Thule, nombre antiguo de Escandinavia. (¿Pero porqué Tm?)
Lutecio (Lu): de Lutetia, antiguo nombre de Pans.
Hafnio (Hf): de Hafnia, nombre latín de Copenhague.
Polonio (Po): de Polonia, en honor de Marie Curie (polaca) codescubridora del elemento junto con su marido Pierre.
Francio (Fr): de Francia.
Americio (Am): de América.
Berkelio (Bk): de Berkeley, universidad de California.
Californio (Cf): de California (estado estadounidense).
Renio (Re): del latín Rhenus, Rin.
Nombres que hacen referencia a propiedades:
Scandio (Sc) Scandia, Escandinavia ( por cierto, Vanadio (V): Vanadis, diosa escandinava).
Cobre (Cu): cuprum, de la isla de Chipre.
Galio (Ga): de Gallia, Francia.
Germanio(Ge): de Germania, Alemania.
Selenio (Se):de Selene, la Luna.
Estroncio (Sr): Strontian, ciudad de Escocia.
Itrio (Y): de Ytterby, pueblo de Suecia.
Rutenio (Ru): del latín Ruthenia, Rusia.
Terbio (Tb): de Ytterby, pueblo de Suecia.
Europio (Eu): de Europa.
Holmio (Ho): del latín Holmia, Estocolmo.
Tulio (Tm): de Thule, nombre antiguo de Escandinavia. (¿Pero porqué Tm?)
Lutecio (Lu): de Lutetia, antiguo nombre de Pans.
Hafnio (Hf): de Hafnia, nombre latín de Copenhague.
Polonio (Po): de Polonia, en honor de Marie Curie (polaca) codescubridora del elemento junto con su marido Pierre.
Francio (Fr): de Francia.
Americio (Am): de América.
Berkelio (Bk): de Berkeley, universidad de California.
Californio (Cf): de California (estado estadounidense).
Renio (Re): del latín Rhenus, Rin.
Nombres que hacen referencia a propiedades:
Berilio (Be) de beriio, esmeralda de color verde.
Hidrógneno (H): engendrador de agua.
Nitrógeno (N). engendrador de nitratos (nitrum)
Oxígeno (O): formador de ácidos (oxys)
Cloro (Cl) del griego chloros (amarilio verdoso).
Argón (Ar) argos, inactivo. (Ya sabes, los gases nobles son poco reactivos).
Cromo (Cr): del griego chroma, color.
Manganeso (Mg): de magnes, magnético.
Bromo (Br): del griego bromos, hedor, peste.
Zinc (Zn): del aleman zink, que significa origen oscuro.
Arsenico (As): arsenikon, oropimente amarillo (auripigmentum).
Zirconio (Zr): del árabe zargun, color dorado.
Rubidio (Rb): de rubidius, rojo muy intenso (a la llama).
Rodio (Rh): del griego rhodon, color rosado.
Yodo (I): del griego iodes, violeta.
Indio (In): debido al color indigo (anil) que se observa en su espectro.
Cesio (Cs): de caesius, color azul celeste.
Disprosio (Dy): del griego dysprositos, volverse duro. (Si alguien conoce la razón que me lo haga saber).
Osmio (Os): del griego osme, olor (debido al fuerte olor del OsO4).
Iridio (Ir): de arco iris.
El platino (Pt) en estado metálico es blanquecino y medianamente similar a la plata (aunque mucho menos maleable que esta), por lo que cuando en 1748 el español don Antonio de Ulloa lo encontró en una expedición por Sudamérica lo llamó "platina", lo que quiere decir más o menos "parecido a la plata". Se describe en un obra: "Relación Histórica del viaje a la América Meridional" (Madrid,1748) como sigue:
Hidrógneno (H): engendrador de agua.
Nitrógeno (N). engendrador de nitratos (nitrum)
Oxígeno (O): formador de ácidos (oxys)
Cloro (Cl) del griego chloros (amarilio verdoso).
Argón (Ar) argos, inactivo. (Ya sabes, los gases nobles son poco reactivos).
Cromo (Cr): del griego chroma, color.
Manganeso (Mg): de magnes, magnético.
Bromo (Br): del griego bromos, hedor, peste.
Zinc (Zn): del aleman zink, que significa origen oscuro.
Arsenico (As): arsenikon, oropimente amarillo (auripigmentum).
Zirconio (Zr): del árabe zargun, color dorado.
Rubidio (Rb): de rubidius, rojo muy intenso (a la llama).
Rodio (Rh): del griego rhodon, color rosado.
Yodo (I): del griego iodes, violeta.
Indio (In): debido al color indigo (anil) que se observa en su espectro.
Cesio (Cs): de caesius, color azul celeste.
Disprosio (Dy): del griego dysprositos, volverse duro. (Si alguien conoce la razón que me lo haga saber).
Osmio (Os): del griego osme, olor (debido al fuerte olor del OsO4).
Iridio (Ir): de arco iris.
El platino (Pt) en estado metálico es blanquecino y medianamente similar a la plata (aunque mucho menos maleable que esta), por lo que cuando en 1748 el español don Antonio de Ulloa lo encontró en una expedición por Sudamérica lo llamó "platina", lo que quiere decir más o menos "parecido a la plata". Se describe en un obra: "Relación Histórica del viaje a la América Meridional" (Madrid,1748) como sigue:
"En el partido de Chocó, habiendo muchas minas de lavadero, como las que se acaban de explicar, se encuentran también algunas, donde por estar disfrazado, y envuelto el oro con otros cuerpos metálicos, jugos y piedras, necesita para su beneficio del auxilio del azogue [mercurio]; y tal vez se hallan minerales, donde la platina (piedra de tanta resistencia, que no es fácil romperla, ni desmenuzarla con la fuerza del golpe sobre el yunque de acero) es causa de que se abandonen; por que ni la calcinación la vence, ni hay arbitrio para extraer el metal, que encierra, sino a expensas de mucho trabajo y costo."
Oro (Au): de aurum, aurora respiandeciente.
Talio (Tl): del griego thallos, vástago o retoño verde.
Bismuto (Bi): del alemán weisse masse, masa blanca.
Astato (At): del griego astatos, inestable.
Radón (Rn): radium emanation (radiactiva). (De noble nada de nada, es radioactivo).
Radio (Ra): del latín radius, rayo.
Actinio (Ac): del griego aktinos, destello o rayo.
Volframio (W): del inglés wolfrahm; o tungsteno, de tung sten, del sueco, piedra pesada.
Bario (Ba): del griego barys, pesado.
Praseodimio (Pr): de prasios, verde, y didymos, gemelo.
Nombre que hacen referencia a la mitología:
Talio (Tl): del griego thallos, vástago o retoño verde.
Bismuto (Bi): del alemán weisse masse, masa blanca.
Astato (At): del griego astatos, inestable.
Radón (Rn): radium emanation (radiactiva). (De noble nada de nada, es radioactivo).
Radio (Ra): del latín radius, rayo.
Actinio (Ac): del griego aktinos, destello o rayo.
Volframio (W): del inglés wolfrahm; o tungsteno, de tung sten, del sueco, piedra pesada.
Bario (Ba): del griego barys, pesado.
Praseodimio (Pr): de prasios, verde, y didymos, gemelo.
Nombre que hacen referencia a la mitología:
Vanadio (V): Vanadis, diosa Escandinava.
Niobio (Nb): Níobe, hija de Tántalo.
Paladio (Pd): Pallas, diosa de la sabiduria.
Prometio (Pm): de Prometeo, personaje mitológico.
Tantalio (Ta): de Tántalo (mitología). (Mira lo que significa y dime si sabes porqué le pusieron este nombre).
Torio (Th): de Thor, dios de la guerra escandinavo. ¡Mira que dar el nombre de un dio guerrero a un elemento!
Vanadio (V): Vanadis, diosa escandinava.
Nombres de científicos:
Niobio (Nb): Níobe, hija de Tántalo.
Paladio (Pd): Pallas, diosa de la sabiduria.
Prometio (Pm): de Prometeo, personaje mitológico.
Tantalio (Ta): de Tántalo (mitología). (Mira lo que significa y dime si sabes porqué le pusieron este nombre).
Torio (Th): de Thor, dios de la guerra escandinavo. ¡Mira que dar el nombre de un dio guerrero a un elemento!
Vanadio (V): Vanadis, diosa escandinava.
Nombres de científicos:
Curio (Cm): en honor de Pierre y Marie Curie.
Einstenio (Es): en honor de Albert Einstein.
Fermio (Fm): en honor de Enrico Fermi.
Mendelevio (Md): En honor al químico ruso Dmitri Ivánovich Mendeléiev precursor de la actual tabla periódica.
Nobelio (No): en honor de Alfred Nobel.
Lawrencio (Lr): en honor de E.O. Lawrence.
Unnilquadium (Unq): Unnilquadium significa 104 (su número atómico) en latín. Los soviéticos propusieron el nombre de Kurchatovium (Ku) en honor de Igor V. Kurchatov, mientras que los estadounidenses preferían el nombre de Rutherfordium (Rf) en honor de Ernest Rutherford. La IUPAC le asignó este nombre temporal en 1980.
Unnilpentium (Unp): en latín unnilpentium equivale a 105 (su número atómico). La IUPAC estableció este nombre frente a las propuestas estadounidenses de llamarlo Hahnio (Ha) en honor de Otto Hahn y de los soviéticos de llamarlo Nielsbohrium en honor de Niels Bohr. (Desde hace un tiempo, la IUPAC utiliza este sistema de nomenclatura para los elementos a partir del 104, hasta que se decida cuales van a ser los nombres definitivos).
Gadolinio (Gd): del mineral gadolinita, del químico finlandés Gadolin.
Samario (Sm): del mineral samarskita, (en honor del ruso Samarski).
Otros:
Einstenio (Es): en honor de Albert Einstein.
Fermio (Fm): en honor de Enrico Fermi.
Mendelevio (Md): En honor al químico ruso Dmitri Ivánovich Mendeléiev precursor de la actual tabla periódica.
Nobelio (No): en honor de Alfred Nobel.
Lawrencio (Lr): en honor de E.O. Lawrence.
Unnilquadium (Unq): Unnilquadium significa 104 (su número atómico) en latín. Los soviéticos propusieron el nombre de Kurchatovium (Ku) en honor de Igor V. Kurchatov, mientras que los estadounidenses preferían el nombre de Rutherfordium (Rf) en honor de Ernest Rutherford. La IUPAC le asignó este nombre temporal en 1980.
Unnilpentium (Unp): en latín unnilpentium equivale a 105 (su número atómico). La IUPAC estableció este nombre frente a las propuestas estadounidenses de llamarlo Hahnio (Ha) en honor de Otto Hahn y de los soviéticos de llamarlo Nielsbohrium en honor de Niels Bohr. (Desde hace un tiempo, la IUPAC utiliza este sistema de nomenclatura para los elementos a partir del 104, hasta que se decida cuales van a ser los nombres definitivos).
Gadolinio (Gd): del mineral gadolinita, del químico finlandés Gadolin.
Samario (Sm): del mineral samarskita, (en honor del ruso Samarski).
Otros:
Helio (He): de la atmostera del sol (helios, se descubrió por primera vez en el espectro de la corona solar durante un eclipse en 1868, aunque la mayoría de los científicos no lo aceptaron hasta que se aisló en la tierra).
Litio (Li): de lithos, roca.
Boro (B): del arabe buraq.
Carbono (C): carbón.
Fluor (F): de fluere (que no se lo que significa)..
Neón (Ne). nuevo (del griego neos). (No se complicaron nada la vida con el nombre).
Sodio (Na): Del latín sodanum (sosa), Na del latín natrium (nitrato de sodio).
Aluminio (Al): del latín alumen (que tampoco se lo que significa).
Silicio (Si): de silex, sílice.
Fósforo (P) de phosphoros, portador de luz (el fosforo emite luz en la obscuridad porque arde al combinarse lentamente con el oxígeno del aire).
Azufre (S) del latín sulphurium.
Potasio (K) kalium; el nombre, del inglés pot ashes (cenizas). (Las cenizas de algunas plantas son ricas en potasio).
Calcio (Ca) de calx, caliza. (La caliza está formada por Ca2CO3).
Hierro (Fe): de ferrum.
Cobalto (Co): He leído dos explicaciones, una que dice que cobalto proviene de cobalos, mina. Otra versión asegura que cobalto es el nombre de un espíritu maligno de la mitología alemana. Lee aquí su historia.
Niquel (Ni): proviene del término alemán kupfernickel, que quiere decir algo asi como cobre del demonio, (aparece en minas de cobre pero no lo es). Como kupfer significa cobre, níquel debe querer decir demonio.
Kriptón (Kr): del griego kryptos, oculto, secreto.
Molibdeno (Mo): de molybdos, plomo. (Al parecer, los primeros químicos lo confundieron con mena de plomo).
Tecnecio (Tc): de technetos, artificial, porque fue uno de los primeros sintetizados.
Plata (Ag): del latín argentum.
Cadmio (Cd): del latín cadmia, nombre antiguo del carbonato de zinc. (Casi todo el cadmio industrial se obtiene como subproducto en el refinado de los minerales de zinc, quizás sea por eso). Si alguien conoce la historia exacta del nombre que me la haga llegar.
Estaño (Sn): del latín stannum.
Antimonio (Sb): de antimonium; Sb de stibium.
Teluro (Te): de Tellus, tierra.
Xenon (Xe): del griego xenon, extraño, raro.
Lantano (La): del griego lanthanein, yacer oculto.
Neodimio (Nd): de neos-dydmos, nuevo gemelo (del lantano).
Plomo (Pb): del latín plumbum.
Protoactinio (Pa): de protos (primero) y actinium.
Litio (Li): de lithos, roca.
Boro (B): del arabe buraq.
Carbono (C): carbón.
Fluor (F): de fluere (que no se lo que significa)..
Neón (Ne). nuevo (del griego neos). (No se complicaron nada la vida con el nombre).
Sodio (Na): Del latín sodanum (sosa), Na del latín natrium (nitrato de sodio).
Aluminio (Al): del latín alumen (que tampoco se lo que significa).
Silicio (Si): de silex, sílice.
Fósforo (P) de phosphoros, portador de luz (el fosforo emite luz en la obscuridad porque arde al combinarse lentamente con el oxígeno del aire).
Azufre (S) del latín sulphurium.
Potasio (K) kalium; el nombre, del inglés pot ashes (cenizas). (Las cenizas de algunas plantas son ricas en potasio).
Calcio (Ca) de calx, caliza. (La caliza está formada por Ca2CO3).
Hierro (Fe): de ferrum.
Cobalto (Co): He leído dos explicaciones, una que dice que cobalto proviene de cobalos, mina. Otra versión asegura que cobalto es el nombre de un espíritu maligno de la mitología alemana. Lee aquí su historia.
Niquel (Ni): proviene del término alemán kupfernickel, que quiere decir algo asi como cobre del demonio, (aparece en minas de cobre pero no lo es). Como kupfer significa cobre, níquel debe querer decir demonio.
Kriptón (Kr): del griego kryptos, oculto, secreto.
Molibdeno (Mo): de molybdos, plomo. (Al parecer, los primeros químicos lo confundieron con mena de plomo).
Tecnecio (Tc): de technetos, artificial, porque fue uno de los primeros sintetizados.
Plata (Ag): del latín argentum.
Cadmio (Cd): del latín cadmia, nombre antiguo del carbonato de zinc. (Casi todo el cadmio industrial se obtiene como subproducto en el refinado de los minerales de zinc, quizás sea por eso). Si alguien conoce la historia exacta del nombre que me la haga llegar.
Estaño (Sn): del latín stannum.
Antimonio (Sb): de antimonium; Sb de stibium.
Teluro (Te): de Tellus, tierra.
Xenon (Xe): del griego xenon, extraño, raro.
Lantano (La): del griego lanthanein, yacer oculto.
Neodimio (Nd): de neos-dydmos, nuevo gemelo (del lantano).
Plomo (Pb): del latín plumbum.
Protoactinio (Pa): de protos (primero) y actinium.
Tabla periódica y su historia
|
Los químicos se dieron cuenta desde los comienzos del desarrollo de la Química, que ciertos elementos tienen propiedades semejantes.
En 1829 el químico alemán Döbereiner realizo el primer intento de establecer una ordenación en los elementos químicos, haciendo notar en sus trabajos las similitudes entre los elementos cloro, bromo y iodo por un lado y la variación regular de sus propiedades por otro.
Una de las propiedades que parecía variar regularmente entre estos era el peso atómico. Pronto estas similitudes fueron también observadas en otros casos, como entre el calcio, estroncio y bario. Una de las propiedades que variaba con regularidad era de nuevo el peso atómico. Ahora bien, como el concepto de peso atómico aún no tenía un significado preciso y Döbereiner no había conseguido tampoco aclararlo y como había un gran número de elementos por descubrir, que impedían establecer nuevas conexiones, sus trabajos fueron desestimados.
Desde 1850 hasta 1865 se descubrieron muchos elementos nuevos y se hicieron notables progresos en la determinación de las masas atómicas, además, se conocieron mejor otras propiedades de los mismos.
Fue en 1864 cuando estos intentos dieron su primer fruto importante, cuando Newlands estableció la ley de las octavas. Habiendo ordenado los elementos conocidos por su peso atómico y después de disponerlos en columnas verticales de siete elementos cada una, observó que en muchos casos coincidían en las filas horizontales elementos con propiedades similares y que presentaban una variación regular.
Esta ordenación, en columnas de siete da su nombre a la ley de las octavas, recordando los periodos musicales. En algunas de las filas horizontales coincidían los elementos cuyas similitudes ya había señalado Döbereiner. El fallo principal que tuvo Newlands fue el considerar que sus columnas verticales (que serían equivalentes a períodos en la tabla actual) debían tener siempre la misma longitud. Esto provocaba la coincidencia en algunas filas horizontales de elementos totalmente dispares y tuvo como consecuencia el que sus trabajos fueran desestimados.
En 1869 el químico alemán Julius Lothar Meyer y el químico ruso Dimitri Ivanovich Mendelyev propusieron la primera “Ley Periódica”.
Meyer al estudiar los volúmenes atómicos de los elementos y representarlos frente al peso atómico observó la aparición en el gráfico de una serie de ondas. Cada bajada desde un máximo (que se correspondía con un metal alcalino) y subido hasta el siguiente, representaba para Meyer un periodo. En los primeros periodos, se cumplía la ley de las octavas, pero después se encontraban periodos mucho más largos. Aunque el trabajo de Meyer era notablemente meritorio, su publicación no llego a tener nunca el reconocimiento que se merecía, debido a la publicación un año antes de otra ordenación de los elementos que tuvo una importancia definitiva.
Utilizando como criterio la valencia de los distintos elementos, además de su peso atómico, Mendelyev presentó su trabajo en forma de tabla en la que los periodos se rellenaban de acuerdo con las valencias (que aumentaban o disminuían de forma armónica dentro de los distintos periodos) de los elementos.
Esta ordenación daba de nuevo lugar a otros grupos de elementos en los que coincidían elementos de propiedades químicas similares y con una variación regular en sus propiedades físicas.
La tabla explicaba las observaciones de Döbereiner, cumplía la ley de las octavas en sus primeros periodos y coincidía con lo predicho en el gráfico de Meyer. Además, observando la existencia de huecos en su tabla, Mendelyev dedujo que debían existir elementos que aun no se habían descubierto y además adelanto las propiedades que debían tener estos elementos de acuerdo con la posición que debían ocupar en la tabla.
Años más tarde, con el descubrimiento del espectrógrafo, el descubrimiento de nuevos elementos se aceleró y aparecieron los que había predicho Mendelyev. Los sucesivos elementos encajaban en esta tabla. Incluso la aparición de los gases noblesencontró un sitio en esta nueva ordenación.
La tabla de Mendelyev fue aceptada universalmente y hoy, excepto por los nuevos descubrimientos relativos a las propiedades nucleares y cuánticas, se usa una tabla muy similar a la que él elaboró más de un siglo atrás.
Los últimos cambios importantes en la tabla periódica son el resultado de los trabajos de Glenn Seaborg a mediados del siglo XX, empezando con su descubrimiento del plutonio en 1940 y, posteriormente, el de los elementos transuránidos del 94 al 102 (Plutonio, Pu; Americio, Am; Curio, Cm; Berkelio, Bk; Californio, Cf; Einstenio, Es; Fermio, Fm; Mendelevio, Md; y Nobelio, No).
Seaborg, premio Nobel de Química en 1951, reconfiguró la tabla periódica poniendo la serie de los actínidos debajo de la serie de los lantánidos.
Seaborg, premio Nobel de Química en 1951, reconfiguró la tabla periódica poniendo la serie de los actínidos debajo de la serie de los lantánidos.
En las tablas escolares suele representarse el símbolo, el nombre, el número atómico y la masa atómica de los elementos como datos básicos y, según su complejidad, algunos otros datos sobre los elementos
Utilidad de la tablaOtra clasificación que resulta importante conocer y es de gran utilidad en la nomenclatura es la que nos brinda información sobre la capacidad de combinación de los elementos o sea su valencia así como su estado o número de oxidación.Existe una clasificación que ubica a los elementos representativos en ocho grupos identificados como A y a los de transición en B. Los elementos representativos son conocidos así porque el número de grupos representa la cantidad de electrones en su capa de valencia o sea el último nivel, y la cantidad de electrones en esa capa nos indica la valencia máxima que el elemento puede presentar.La valencia de un elemento se refiere a la capacidad de combinación que presenta; en el caso de los no metales se relaciona con el número de átomos de hidrógeno con que se puede enlazar y en los metales con cuántos átomos de cloro se une.Ejemplos:El Calcio se puede unir a dos átomos de Cloro por lo que su valencia es dos. CaCl2El Oxígeno forma agua uniéndose a dos hidrógenos, su valencia también será dos. H2OEl Nitrógeno se une a tres Hidrógenos en la formación de Amoníaco, su valencia es tres. NH3En la nomenclatura de las sustancias inorgánicas resulta de mayor importancia aún conocer el estado de oxidación, este regularmente es la valencia con un signo que expresa la carga adquirida por el elemento al enlazarse con otros diferentes a él; es decir, átomos de distinta electronegatividad. El estado o número de oxidación generalmente expresa la cantidad de electrones que un átomo aporta en la formación de enlaces con otros átomos de elementos diferentes. (Ver: PSU: Química, Pregunta 02_2005)Ejemplos:El calcio se une al cloro formando el compuesto CaCl2; en este caso el Calcio tiene estado de oxidación +2 ya que emplea dos electrones al unirse con el Cloro quien presenta -1, al emplear sólo un electrón.El oxígeno forma agua al unirse con un estado de oxidación de -2 con el hidrógeno que presenta +1.Existen compuestos que nos permiten establecer diferencias entre valencia y número de oxidación.Ejemplos:El oxígeno al formarse el peróxido de hidrógeno (agua oxigenada) presenta valencia dos mientras que su número de oxidación es -1; su fórmula es H2O2 y puede representarse con una estructura en donde se aprecia que cada oxígeno solo emplea un electrón para unirse al Hidrógeno quien sería el átomo diferente; sin embargo, son dos los enlaces que forma.
Períodos
En la tabla periódica los elementos están ordenados de forma que aquellos con propiedades químicas semejantes, se encuentren situados cerca uno de otro.
Los elementos se distribuyen en filas horizontales, llamadas períodos. Pero los periodos no son todos iguales, sino que el número de elementos que contienen va cambiando, aumentando al bajar en la tabla periódica.
El primer periodo tiene sólo dos elementos, el segundo y tercer periodo tienen ocho elementos, el cuarto y quinto periodos tienen dieciocho, el sexto periodo tiene treinta y dos elementos, y el séptimo no tiene los treinta y dos elementos porque está incompleto. Estos dos últimos periodos tienen catorce elementos separados, para no alargar demasiado la tabla y facilitar su trabajo con ella.
El periodo que ocupa un elemento coincide con su última capa electrónica. Es decir, un elemento con cinco capas electrónicas, estará en el quinto periodo. El hierro, por ejemplo, pertenece al cuarto periodo, ya que tiene cuatro capas electrónicas.
CLASIFICACIÓN DE LOS ELEMENTOS QUÍMICOS
La clasificación más fundamental de los elementos químicos es en metales y no metales.
Los metales se caracterizan por su apariencia brillante, capacidad para cambiar de forma sin romperse (maleables) y una excelente conductividad del calor y la electricidad.
Los no metales se caracterizan por carecer de estas propiedades físicas aunque hay algunas excepciones (por ejemplo, el yodo sólido es brillante; el grafito, es un excelente conductor de la electricidad; y el diamante, es un excelente conductor del calor).
Las características químicas son: los metales tienden a perder electrones para formar iones positivos y los no metales tienden a ganar electrones para formar iones negativos. Cuando un metal reacciona con un no metal, suele producirse transferencia de uno o más electrones del primero al segundo.
Propiedad de los metales
Poseen bajo potencial de ionización y alto peso específico
Por regla general, en su último nivel de energía tienen de 1 a 3 electrones.
Son sólidos a excepción del mercurio (Hg), galio (Ga), cesio (Cs) y francio (Fr), que son líquidos
Presentan aspecto y brillo metálicos
Son buenos conductores del calor y la electricidad
Son dúctiles y maleables, algunos son tenaces, otros blandos
Se oxidan por pérdida de electrones
Su molécula está formada por un solo átomo, su estructura cristalina al unirse con el oxígeno forma óxidos y éstos al reaccionar con el agua forman hidróxidos
Los elementos alcalinos son los más activos
Propiedades generales de los no-metales
Tienen tendencia a ganar electrones
Poseen alto potencial de ionización y bajo peso específico
Por regla general, en su último nivel de energía tienen de 4 a 7 electrones
Se presentan en los tres estados físicos de agregación
No poseen aspecto ni brillo metálico
Son malos conductores de calor y la electricidad
No son dúctiles, ni maleables, ni tenaces
Se reducen por ganancia de electrones
Sus moléculas están formadas por dos o más átomos
Al unirse con el oxígeno forman anhídridos y éstos al reaccionar con el agua, forman oxiácidos
Los halógenos y el oxígeno son los más activos
Varios no-metales presentan alotropía
La mayoría de los elementos se clasifican como metales. Los metales se encuentran del lado izquierdo y al centro de la tabla periódica. Los no metales, que son relativamente pocos, se encuentran el extremo superior derecho de dicha tabla. Algunos elementos tienen comportamiento metálico y no metálico y se clasifican como metaloides y semimetales.
Los no metales también tienen propiedades variables, al igual que los metales. En general los elementos que atraen electrones de los metales con mayor eficacia se encuentran en el extremo superior derecho de la tabla periódica.
Breve descripción de las propiedades y aplicaciones de algunos elementos de la Tabla Periódica.
Gases nobles o gases raros
Los gases nobles, llamados también raros o inertes, entran, en escasa proporción, en la composición del aire atmosférico. Pertenecen a este grupo el helio, neón, argón, criptón, xenón y radón, que se caracterizan por su inactividad química, puesto que tienen completos sus electrones en la última capa. No tienen tendencia por tanto, ni a perder ni a ganar electrones. De aquí que su valencia sea cero o que reciban el nombre de inertes, aunque a tal afirmación se tiene hoy una reserva que ya se han podido sintetizar compuestos de neón, xerón o kriptón con el oxígeno, el flúor y el agua.
El helio se encuentra en el aire; el neón y el kriptón se utilizan en la iluminación por sus brillantes colores que emiten al ser excitados, el radón es radioactivo.
Familias de la Tabla
Periódica
Colocados en
orden creciente de número atómico, los elementos pueden agruparse, por el
parecido de sus propiedades, en 18 familias o grupos (columnas verticales).
Desde el punto de vista electrónico, los elementos de una familia poseen la
misma configuración electrónica en
la última capa, aunque difieren en el número de capas (periodos). Los grupos o
familias son 18 y se corresponden con las columnas de la Tabla Periódica. A
continuación se muestran las propiedades generales de los grupos
representativos (zona de llenado de orbitales s y p) y
las de otras agrupaciones de elementos que se pueden hacer teniendo en cuenta
la zona de llenado de orbitales d (transición), f (tierras raras), el carácter
metálico (metal, no metal, metaloide).
Los metales alcalinos son aquellos que se encuentran en el primer grupo dentro de la tabla periódica.
Con excepción del hidrógeno, son todos blancos, brillantes, muy activos, y se les encuentra combinados en forma de compuestos. Se les debe guardar en la atmósfera inerte o bajo aceite.
Los compuestos de los metales alcalinos son isomorfos, lo mismo que los compuestos salinos del amonio. Este radical presenta grandes analogías con los metales de este grupo.
Estos metales, cuyos átomos poseen un solo electrón en la capa externa, son monovalentes. Dada su estructura atómica, ceden fácilmente el electrón de valencia y pasan al estado iónico. Esto explica el carácter electropositivo que poseen, así como otras propiedades.
Los de mayor importancia son el sodio y el potasio, sus sales son empleadas industrialmente en gran escala.
Metales alcalinos
Los metales alcalinos corresponden al Grupo 1 de la Tabla Periódica (anteriormente grupo I A).
Átomo de litio.
Estos metales son: Litio (Li), sodio (Na), potasio (K), rubidio (Rb), cesio (Cs)y francio (Fr).
Constituyen el 4,8 por ciento de la corteza terrestre, incluyendo capa acuosa y atmósfera. El sodio y el potasio son los más abundantes; el resto es raro.
El nombre de esta familia proviene de la palabra árabe álcalis, que significacenizas; ya que los primeros compuestos de sodio y potasio fueron descubiertos en cenizas de maderas.
También, al reaccionar con agua, estos metales forman hidróxidos, que son compuestos que antes se llamaban álcalis.
Son metales blandos, tan es así que el sodio se puede cortar fácilmente con un cuchillo. Al cortarlos o fundirlos se observa su color plateado y su brillo metálico.
Los metales alcalinos son de baja densidad. Li, Na y K son menos densos que el agua. El Li es el más duro y a la vez el menos denso. El Cs es el más blando y el más denso.
Son blanco-plateados, con puntos de fusión bajos (debido a las fuerzas de enlace débiles que unen sus átomos) que decrecen según se desciende en el grupo y blandos, siendo el litio el más duro. Sus puntos de fusión bajos están comprendidos entre 181º C para el Li y 28,7º C para el Cs.
Estos metales son los más reactivos químicamente. Por ejemplo: el sodio reacciona enérgicamente con el agua, mientras flota, desprendiéndose gases de hidrógeno. El potasio reacciona aún más violentamente que el sodio.
Átomo de sodio.
Por estos motivos, esta clase de metales no se encuentran en estado libre en la naturaleza, sino en forma de compuestos, generalmente sales.
Los elementos sodio y potasio son componentes fundamentales de los seres vivos. Se encuentran en forma de iones, cuyas propiedades son muy diferentes a la de los metalesEl NaCl (cloruro de sodio) es el soluto más abundante en el agua del mar. El KNO3 (nitrato de potasio) es el salitre, y abunda en algunos yacimientos, especialmente en Chile.
Grandes depósitos naturales de compuestos de litio se encuentran en el fondo de lagos que se secaron.
El rubidio y el cesio son muy escasos. El francio es altamente radiactivo y de muy corta vida (22 minutos), por lo que es mucho más escaso aún.
Su configuración electrónica muestra un electrón en su capa de valencia (1 electrón s).
Son muy electropositivos: baja energía de ionización. Por tanto, pierden este electrón fácilmente (número de oxidación +1) y se unen mediante enlace iónico con otros elementos.
En estado sólido forman redes cúbicas.
Como el resto de los metales, los metales alcalinos son maleables, dúctiles y buenos conductores del calor y la electricidad.
Presentan efecto fotoeléctrico con radiación de baja energía, siendo más fácil de ionizar el cesio. La reactividad aumenta hacia abajo, siendo el cesio y el francio los más reactivos del grupo.
El litio se parece bastante más al magnesio en cuanto a reactividad que al resto de los alcalinos, debido a que el ion Li+ es muy pequeño.
Los metales alcalinos se recubren rápidamente de una capa de hidróxido en contacto con el aire y reaccionan violentamente en contacto con el agua, liberando hidrógeno que, debido al calor desprendido, arde (con rubidio y cesio la reacción es explosiva, ya que al ser más densos que el agua, la reacción la producen en el fondo y el hidrógeno formado arde produciendo una onda de choque que puede romper el recipiente).
También reaccionan con el vapor de agua del aire o con la humedad de la piel. Deben guardarse en líquidos apolares anhidros.
Líquidos apolares son aquellos cuyas moléculas no presentan polarización, siendo de este modo hidrófugos (no se mezclan con el agua). Apolares son, por ejemplo, el aceite, el metano.
Lepidolita, una de las mayores fuentes del raro rubidio y del cesio.
Son reductores poderosos, sus óxidos son básicos así como sus hidróxidos. Reaccionan directamente con los halógenos, el hidrógeno, el azufre y el fósforo originando los haluros, hidruros, sulfuros y fosfuros correspondientes.
Con el amoníaco líquido dan soluciones de color azul en las que hay electrones libres ocupando cavidades formadas por moléculas de amoníaco; estas soluciones se emplean para reducir compuestos orgánicos. Según aumenta la concentración de metal, la solución toma color bronce y empieza a conducir la electricidad.
Casi todas las sales son solubles en agua, siendo menos solubles las de litio.
Se emplean como refrigerantes líquidos en centrales nucleares (litio, sodio, potasio) y como conductores de corriente dentro de un revestimiento plástico.
Sus compuestos tienen un gran número de aplicaciones.
Grupo II, metales alcalinotérreos
Se conocen con el nombre de metales alcalinotérreos los seis elementos que forman el grupo IIA del sistema periódico: berilio, magnesio, calcio, estroncio, bario y radio. Son bivalentes y se les llama alcalinotérreos a causa del aspecto térreo de sus óxidos.
El radio es un elemento radiactivo.
Estos elementos son muy activos aunque no tanto como los del grupo I. Son buenos conductores del calor y la electricidad, son blancos y brillantes.
Como el nombre indica, manifiestan propiedades intermedias entre los metales alcalinos y los térreos; el magnesio y, sobre todo, el berilio son los que más se asemejan a estos.
No existen en estado natural, por ser demasiado activos y, generalmente, se presentan formando silicatos, carbonatos, cloruros y sulfatos, generalmente insolubles.
Estos metales son difíciles de obtener, por lo que su empleo es muy restringido.
Metales alcalinotérreos
Serie de seis elementos químicos que se encuentran en el grupo 2 (o II A) del sistema periódico.
Presentación de alcalinotérreos.
Los metales alcalinotérreos son, por orden de número atómico creciente:berilio (Be), magnesio (Mg), calcio (Ca), estroncio (Sr), bario (Ba) y radio (Ra).
Sus óxidos se llaman tierras alcalinas.
Estado natural y abundancia
Berilio: silicatos: fenacita y berilio. No muy familiar y difícil de extraer
Magnesio: sales en el agua del mar y magnesita
Calcio: calcita, dolomita y yeso
Estroncio: celestita y estroncianita. Concentrados en menas y fácil de extraer
Bario: baritas. Concentrados en menas y fácil de extrae
Radio: escaso y radiactivo
Propiedades físicas
Color blanco plateado, de aspecto lustroso y blandos. El magnesio es gris por una película superficial de óxidos.
Aunque son bastante frágiles, los metales alcalinotérreos son maleables y dúctiles.
Conducen bien la electricidad y cuando se calientan arden fácilmente en el aire.
Tamaño y densidad: Gran tamaño atómico. La carga nuclear efectiva es más elevada y hay una mayor contracción de los orbitales atómicos. Más densos.
Dureza y punto de fusión: Tienen dos electrones de valencia que participan en el enlace metálico, por lo que son más duros. Puntos de fusión más elevados y no varían de forma regular debido a las diferentes estructuras cristalinas.
Propiedades químicas
Son menos reactivos que los metales alcalinos, pero lo suficiente como para no existir libres en la naturaleza.
Menos electropositivos y más básico. Forman compuestos iónicos. El berilio muestra diferencias significativas con los restos de los elementos.
La energía de ionización más alta es compensada por las energías de hidratación o energías reticulares.
Compuestos diamagnéticos e incoloros. Son poderosos agentes reductores, es decir, se desprenden fácilmente de los electrones.
Grupo III, familia del boro
El boro es menos metálico que los demás. El aluminio es anfótero. El galio, el indio y el talio son raros y existen en cantidades mínimas. El boro tiene una amplia química de estudio.
Grupo IV, Familia del carbono
El estudio de los compuestos del carbono corresponde a la Química Orgánica. El carbono elemental existe como diamante y grafito.
El silicio comienza a ser estudiado ampliamente por su parecido con el carbono. Los elementos restantes tienen más propiedades metálicas.
Carbono
Descripción
Nombre
Carbono
Número atómico
Valencia
Configuración electrónica
1s22s22p2
Masa atómica (g/mol)
12,01115
Densidad (g/ml)
2,26
Punto de ebullición (ºC)
4830
Punto de fusión (ºC) 3727
Descubridor
Los antiguos carbono, de símbolo C, es un elemento crucial para la existencia de los organismos vivos, y que tiene muchas aplicaciones industriales importantes. Su número atómico es 6; y pertenece al grupo 14 (o IV A) del sistema periódico.
Propiedades
Átomo de carbono.
Las propiedades físicas y químicas del carbono dependen de la estructura cristalina del elemento.
Un gran número de metales se combinan con el elemento a temperaturas elevadas para formar carburos.
Con el oxígeno forma tres compuestos gaseosos: monóxido de carbono, CO, dióxido de carbono, CO2, y subóxido de carbono, C3O2.
Los dos primeros son los más importantes desde el punto de vista industrial.
El carbono es un elemento único en la química porque forma un número de compuestos mayor que la suma total de todos los otros elementos combinados.
El grupo más grande de estos compuestos es el constituido por carbono e hidrógeno. Se estima que se conoce un mínimo de 1.000.000 de compuestos orgánicos y este número crece rápidamente cada año. Aunque la clasificación no es rigurosa, el carbono forma otra serie de compuestos considerados como inorgánicos, en un número mucho menor al de los orgánicos.
Las tres formas de carbono elemental existentes en la naturaleza (diamante, grafito y carbono amorfo) son sólidos con puntos de fusión extremadamente altos, e insolubles en todos los disolventes a temperaturas ordinarias. Las propiedades físicas de las tres formas difieren considerablemente a causa de las diferencias en su estructura cristalina
En el diamante, el material más duro que se conoce, cada átomo está unido a otros cuatro en una estructura tridimensional, mientras que el grafito consiste en láminas débilmente unidas de átomos dispuestos en hexágonos.
El carbono químicamente puro se prepara por descomposición térmica del azúcar (sacarosa) en ausencia de aire.
El carbono tiene la capacidad única de enlazarse con otros átomos de carbono para formar compuestos en cadena y cíclicos muy complejos. Esta propiedad conduce a un número casi infinito de compuestos de carbono, siendo los más comunes los que contienen carbono e hidrógeno.
Pieza de carbono.
Sus primeros compuestos fueron identificados a principios del siglo XIX en la materia viva, y, debido a eso, el estudio de los compuestos de carbono se denominó química orgánica.
A temperaturas normales, el carbono se caracteriza por su baja reactividad. A altas temperaturas, reacciona directamente con la mayoría de los metales formando carburos, y con el oxígeno formando monóxido de carbono (CO) y dióxido de carbono (CO2).
El carbono en forma de coque se utiliza para eliminar el oxígeno de las menas que contienen óxidos de metales, obteniendo así el metal puro. El carbono forma también compuestos con la mayoría de los elementos no metálicos, aunque algunos de esos compuestos, como el tetracloruro de carbono (CCl4), han de ser obtenidos indirectamente.
Estado natural
El carbono es un elemento ampliamente distribuido en la naturaleza, aunque sólo constituye un 0,025% de la corteza terrestre, donde existe principalmente en forma de carbonatos.
Varios minerales, como caliza, dolomita, yeso y mármol, tienen carbonatos.
Todas las plantas y animales vivos están formados de compuestos orgánicos complejos en donde el carbono está combinado con hidrógeno, oxígeno, nitrógeno y otros elementos.
Los vestigios de plantas y animales vivos forman depósitos: de petróleo, asfalto y betún. Los depósitos de gas natural contienen compuestos formados por carbono e hidrógeno.
El elemento libre tiene muchos usos, que incluyen desde las aplicaciones ornamentales del diamante en joyería hasta el pigmento de negro de humo en llantas de automóvil y tintas de imprenta.
Otra forma del carbono, el grafito, se utiliza para crisoles de alta temperatura, electrodos de celda seca y de arco de luz, como puntillas de lápiz y como lubricante. El carbón vegetal, una forma amorfa del carbono, se utiliza como absorbente de gases y agente decolorante.
Los compuestos de carbono tienen muchos usos.
Diamante.
El dióxido de carbono se utiliza en la carbonatación de bebidas, en extintores de fuego y, en estado sólido, como enfriador (hielo seco). El monóxido de carbono se utiliza como agente reductor en muchos procesos metalúrgicos. El tetracloruro de carbono y el disulfuro de carbono son disolventes industriales importantes. El freón se utiliza en aparatos de refrigeración. El carburo de calcio se emplea para preparar acetileno; es útil para soldar y cortar metales, así como para preparar otros compuestos orgánicos. Otros carburos metálicos tienen usos importantes como refractarios y como cortadores de metal.
El dióxido de carbono es un componente importante de la atmósfera y la principal fuente de carbono que se incorpora a la materia viva. Por medio de la fotosíntesis, los vegetales convierten el dióxido de carbono en compuestos orgánicos de carbono, que posteriormente son consumidos por otros organismos.
Ver: Ciclo del carbono
El carbono amorfo se encuentra con distintos grados de pureza en el carbón de leña, el carbón, el coque, el negro de carbono y el negro de humo.
El negro de humo, al que a veces se denomina de forma incorrecta negro de carbono, se obtiene quemando hidrocarburos líquidos como el queroseno, con una cantidad de aire insuficiente, produciendo una llama humeante. El humo u hollín se recoge en una cámara separada. Durante mucho tiempo se utilizó el negro de humo como pigmento negro en tintas y pinturas, pero ha sido sustituido por el negro de carbono, que está compuesto por partículas más finas.
El negro de carbono, llamado también negro de gas, se obtiene por la combustión incompleta del gas natural y se utiliza sobre todo como agente de relleno y de refuerzo en el caucho o hule.
En 1985, los científicos volatilizaron el grafito para producir una forma estable de molécula de carbono consistente en 60 átomos de carbono dispuestos en una forma esférica desigual parecida a un balón de fútbol. La molécula recibió el nombre de buckminsterfulereno ('pelota de Bucky' para acortar) en honor a R. Buckminster Fuller, el inventor de la cúpula geodésica. La molécula podría ser común en el polvo interestelar.
Aplicaciones científicas
El isótopo del carbono más común es el carbono 12; en 1961 se eligió este isótopo para sustituir al isótopo oxígeno 16 como medida patrón para las masas atómicas, y se le asignó la masa atómica 12.
Los isótopos carbono 13 y carbono 14 se usan como trazadores (consultar Trazador isotópico) en la investigación bioquímica. El carbono 14 se utiliza también en la técnica llamada método del carbono 14, que permite estimar la edad de los fósiles y otras materias orgánicas. Este isótopo es producido continuamente en la atmósfera por los rayos cósmicos, y se incorpora a toda la materia viva.
Como el carbono 14 se desintegra con un periodo de semidesintegración de 5.760 años, la proporción entre el carbono 14 y el carbono 12 en un espécimen dado, proporciona una medida de su edad aproximada.
Configuración electrónica
El átomo de carbono constituye el elemento esencial de toda la química orgánica, y debido a que las propiedades químicas de elementos y compuestos son consecuencia de las características electrónicas de sus átomos y de sus moléculas, es necesario considerar la configuración electrónica del átomo de carbono para poder comprender su singular comportamiento químico.
Se trata del elemento de número atómico Z = 6. Por tal motivo su configuración electrónica en el estado fundamental o no excitado es 1s2 2s2 2p2. La existencia de cuatro electrones en la última capa sugiere la posibilidad bien de ganar otros cuatro convirtiéndose en el ion C4- cuya configuración electrónica coincide con la del gas noble Ne, bien de perderlos pasando a ion C4+ de configuración electrónica idéntica a la del He.
En realidad una pérdida o ganancia de un número tan elevado de electrones indica una dosis de energía elevada, y el átomo de carbono opta por compartir sus cuatro electrones externos con otros átomos mediante enlaces covalentes. Esa cuádruple posibilidad de enlace que presenta el átomo de carbono se denomina tetravalencia.
El carbono frente al silicio
Cabe preguntarse si la situación del carbono es singular o si por el contrario algún otro elemento participa de sus mismas propiedades. Observando el sistema periódico se advierte que el silicio está situado en el mismo grupo justo debajo del carbono y con idéntica configuración electrónica externa.
¿Por qué razón la vida se ha desarrollado sobre los compuestos del carbono y no sobre los del silicio? ¿Por qué los derivados del silicio son tan poco numerosos frente a los del carbono?
La existencia en el silicio de ocho electrones internos adicionales respecto del carbono hace que los electrones externos o de valencia responsables del enlace químico estén más alejados del núcleo y, por tanto, atraídos por él más débilmente. Ello se traduce en que la fuerza de los enlaces del silicio es comparativamente menor; particularmente lo es el enlace Si-Si, lo que le convierte en más reactivo, es decir, menos estable químicamente.
No obstante, el silicio cristaliza formando una red tridimensional semejante a la del diamante, y sus derivados constituyen el 87 % de la composición de la corteza terrestre. Su combinación con el oxígeno origina la sílice o cuarzo (SiO2). El carácter francamente polar de esta unión da lugar a estructuras reticulares o redes cristalinas que por sus propiedades se parecen enormemente a las de los sólidos iónicos.
La química de compuestos del carbono
El átomo de carbono, debido a su configuración electrónica, presenta una importante capacidad de combinación. Los átomos de carbono pueden unirse entre sí formando estructuras complejas y enlazarse a átomos o grupos de átomos que confieren a las moléculas resultantes propiedades específicas. (Ver: Grupos funcionales)
La enorme diversidad en los compuestos del carbono hace de su estudio químico una importante área del conocimiento puro y aplicado de la ciencia actual.
Durante mucho tiempo la materia constitutiva de los seres vivos estuvo rodeada de no pocas incógnitas. Frente a la materia mineral presentaba, entre otras, una característica singular, su capacidad de combustión. Parecía como si los únicos productos capaces de arder hubieran de proceder de la materia viviente.
En los albores de la química como ciencia se advirtió, además, que si bien la materia procedente de organismos vivos podía degradarse en materia mineral por combustión u otros procesos químicos, no era posible de ninguna manera llevar a cabo en el laboratorio el proceso inverso.
Argumentos de este estilo llevaron a Berzelius, a comienzos del siglo XIX, a sugerir la existencia de dos tipos de materia en la naturaleza, la materia orgánica o materia propia de los seres vivos, y la materia inorgánica.
Para justificar las diferencias entre ambas se admitió que la materia orgánica poseía una composición especial y que su formación era debida a la intervención de una influencia singular o «fuerza vital» exclusiva de los seres vivos y cuya manipulación no era posible en el laboratorio.
La crisis de este planteamiento, denominado vitalismo, llevó consigo el rápido desarrollo de la química de la materia orgánica en los laboratorios, al margen de esa supuesta «fuerza vital».
En la actualidad, superada ya la vieja clasificación de Berzelius, se denomina química orgánica a la química de los derivados del carbono e incluye el estudio de los compuestos en los que dicho elemento constituye una parte esencial, aunque muchos de ellos no tengan relación alguna con la materia viviente.
HIDROCARBUROS: ASPECTOS ESTRUCTURALES
La geometría de sus moléculas.
Los hidrocarburos son los derivados del carbono más sencillos. Resultan de la unión únicamente de átomos de carbono con átomos de hidrógeno y de átomos de carbono entre sí formando cadenas que pueden ser abiertas o cerradas y cuyos «eslabones» pueden estar unidos por enlaces simples o por enlaces múltiples. Aquellos hidrocarburos que presentan únicamente enlaces simples reciben el nombre de hidrocarburos saturados (alcanos).
El representante más sencillo de los hidrocarburos saturados es el metano CH4; no obstante, el etano C2H6 da una mejor idea de las características de este tipo de hidrocarburos.
Etano (un enlace carbono-carbono).
La molécula de etano está compuesta por dos átomos de carbono y seis átomos de hidrógeno que se unen entre sí mediante enlaces covalentes sencillos. Desde un punto de vista puramente geométrico se puede representar la molécula de etano mediante dos tetraedros contiguos y opuestos por uno de sus vértices, en donde los dos átomos de carbono ocupan los centros de los respectivos tetraedros, y los de hidrógeno los vértices libres.
Eteno, dos carbonos con enlace doble.
Los hidrocarburos no saturados se caracterizan, desde el punto de vista de su estructura molecular, por la presencia de enlaces dobles (alquenos) o triples (alquinos). La molécula de eteno o etileno está formada por dos átomos de carbono unidos por un enlace doble; mediante sus otros dos enlaces restantes cada átomo de carbono se une a otros tantos átomos de hidrógeno.
Efectos del Carbono sobre la salud
El carbono elemental es de una toxicidad muy baja. Los datos presentados aquí de peligros para la salud están basados en la exposición al negro de carbono, no carbono elemental. La inhalación continuada de negro de carbón puede resultar en daños temporales o permanentes a los pulmones y el corazón.
Se ha encontrado pneumoconiosis en trabajadores relacionados con la producción de negro de carbón. También se ha dado parte de afecciones cutáneas tales como inflamación de los folículos pilosos, y lesiones de la mucosa bucal debidos a la exposición cutánea.
Carcinogenicidad: El negro de carbón ha sido incluido en la lista de la Agencia Internacional de Investigación del Cáncer (AIIC) dentro del grupo 3 (agente no clasificable con respecto a su carcinogenicidad en humanos).
Grupo V, familia del nitrógeno
Se considera a este grupo como el más heterogéneo de la tabla periódica. El nitrógeno está presente en compuestos tales como las proteínas, los fertilizantes, los explosivos y es constituyente del aire. Como se puede ver, se trata de un elemento tanto benéfico como perjudicial. El fósforo tiene ya una química especial de estudio, sus compuestos son generalmente tóxicos. El arsénico es un metaloide venenoso. El antimonio tiene gran parecido con el aluminio, sus aplicaciones son más de un metal.
Grupo VI, Colágenos
Los cinco primeros elementos son no-metálicos, el último, polonio, es radioactivo. El oxígeno es un gas incoloro constituyente del aire. El agua y la tierra. El azufre es un sólido amarillo y sus compuestos por lo general son tóxicos o corrosivos. La química del teluro y selenio es compleja.
Grupo VII, halógenos
El flúor, el cloro, el bromo, el yodo y el astato, llamados metaloides halógenos, constituyen el grupo de los no metales monovalentes. Todos ellos son coloreados en estado gaseoso y, desde el punto de vista químico, presentan propiedades electronegativas muy acusadas, de donde se deriva la gran afinidad que tienen con el hidrógeno y los metales.
Los formadores de sal se encuentran combinados en la naturaleza por su gran actividad. Las sales de estos elementos con los de los grupos I y II están en los mares. Las propiedades de los halógenos son muy semejantes. La mayoría se sus compuestos derivados son tóxicos, irritantes, activos y tienen gran aplicación tanto en la industria como en el laboratorio.
El astatinio o ástato difiere un poco del resto del grupo.
Elementos de transición
Esta es una familia formada por los grupos IIIB, IVB, VB, VIB, VIIB, IB y IIB, entre los que se encuentran los elementos cobre, fierro, zinc, oro, plata, níquel y platino.
Las características de los metales de transición son muy variadas, algunos se encuentran en la naturaleza en forma de compuestos; otros se encuentran libres
Estos elementos no son tan activos como los representativos, todos son metales y por tanto son dúctiles, maleables, tenaces, con altos puntos de fusión y ebullición, conductores del calor y la electricidad. Poseen orbitales semilleros, y debido a esto es su variabilidad en el estado de oxidación.
Debido al estado de oxidación, los compuestos son coloridos.
ALGUNOS ELEMENTOS QUE CAUSAN CONTAMINACIÓN
En la naturaleza existen algunos elementos que debido a su estructura o en combinación con otros en forma de compuestos, son perjudiciales al hombre, ya que son agentes contaminadores del medio ambiente; en especial del aire, agua y suelo, o bien, porque ocasionan daños irreversibles al ser humano, como la muerte.
Algunos de estos elementos son:
Antimonio (Sb) y textiles.- Se emplea en aleaciones, metal de imprenta, baterías, cerámica. El principal daño que provoca es el envenenamiento por ingestión o inhalación de vapores, principalmente por un gas llamado estibina SbH3.
Arsénico (As) medicamentos y vidrio. Se emplea en venenos para hormigas, insecticidas, pinturas, Es uno de los elementos más venenosos que hay, así como todos los compuestos.
Azufre (S) Principalmente son óxidos SO2 y SO3 contaminan el aire y con agua producen la lluvia ácida. Sustancias tales como derivados clorados de azufre, sulfatos y ácidos son corrosivos. El gas H2S es sumamente tóxico y contamina el aire. El azufre es empleado en algunos medicamentos para la piel.
Bromo (Br) Sus vapores contaminan el aire, además sus compuestos derivados son lacrimógenos y venenosos.
Cadmio (Cd) Metal tóxico que se origina en la refinación del zinc; también proviene de operaciones de electrodeposición y por tanto contamina el aire y el agua. Contenido en algunos fertilizantes contamina el suelo.
Cloro (Cl) Sus valores contaminan el aire y son corrosivos. Se le emplea en forma de cloratos para blanquear la ropa, para lavados bucales y fabricación de cerillos. Los cloratos son solubles en agua y la contaminan, además de formar mezclas explosivas con compuestos orgánicos.
Los valores de compuestos orgánicos clorados como insecticidas, anestésicos y solventes dañan el hígado y el cerebro. Algunos medicamentos que contienen cloro afectan el sistema nervioso.
Cromo (Cr) El cromo y sus compuestos son perjudiciales al organismo, pues destruyen todas las células. Se le emplea en síntesis orgánicas y en la industria del acero. Cualquier cromato solubles contamina el agua.
Magnesio (Mn) Se emplea en la manufactura de acero y de pilas secas. La inhalación de polvos y humos conteniendo magnesio causa envenenamiento. También contamina el agua y atrofia el cerebro.
Mercurio (Hg) Metales de gran utilidad por ser líquidos; se utiliza en termómetros y por ser buen conductos eléctrico se emplea en aparatos de este tipo, así como en iluminación, pinturas fungicidas, catalizadores, amalgamas dentales, plaguicidas, etc. pero contamina el agua, el aire y causa envenenamiento. Las algas lo absorben, luego los peces y finalmente el hombre. Los granos o semillas lo retienen y finalmente el hombre los come.
Plomo (Pb) El plomo se acumula en el cuerpo conforme se inhala del aire o se ingiere con los alimentos y el agua. La mayor parte del plomo que contamina el aire proviene de las gasolinas para automóviles, pues se le agrega para proporcionarle propiedades antidetonantes. También se le emplea en pinturas, como metal de imprenta, soldaduras y acumuladores. Por su uso el organismo se afecta de saturnismo. Sus sales, como el acetato, son venenosas.
Existen otros elementos que de alguna forma contaminan el agua, el aire y el suelo tales como: talio, zinc, selenio, oxígeno de nitrógeno, berilio, cobalto y sobre todo gran cantidad de compuestos que tienen carbono. (Orgánicos).
Aluminio (Al): Metal ligero, resistente a la corrosión y al impacto, se puede laminar e hilar, por lo que se le emplea en construcción, en partes de vehículos, de aviones y en artículos domésticos. Se le extrae de la bauxita.
Azufre (S): No metal, sólido de color amarillo, se encuentra en yacimientos volcánicos y aguas sulfuradas. Se emplea en la elaboración de fertilizantes, medicamentos, insecticidas, productos químicos y petroquímicos.
Cobalto (Co): Metal color blanco que se emplea en la elaboración de aceros especiales debido a su alta resistencia al calor, corrosión y fricción. Se emplea en herramientas mecánicas de alta velocidad, imanes y motores. En forma de polvo se emplea como pigmento azul para el vidrio. Es catalizador. Su isótopo radiactivo se emplea como pigmento azul para el vidrio. Es catalizador
Cobre (Cu): Metal de color rojo que se carbonata al aire húmedo y se pone verde, conocido desde la antigüedad. Se emplea principalmente como conductor eléctrico, también para hacer monedas y en aleaciones como el latón y el bronce.
Hierro (Fe): Metal dúctil, maleable de color gris negruzco, se oxida al ocntacto con el aire húmedo. Se extrae de minerales como la hematina, limonita, pirita, magnetita y siderita. Se le emplea en la industria arte y medicina. Para fabricar acero, cemento, fundiciones de metales no ferrosos nuestra sangre lo contiene en la hemoglobina.
Flúor (F): Este no metal esta contenido en la fluorita CaF2 en forma de vetas encajonadas en calizas. La florita se emplea como fundente en hornos metalúrgicos. Para obtener HF, NHF4 y grabar el vidrio; también en la industria química, cerámica y potabilización del agua.
Fósforo (P): Elemento no metálico que se encuentra en la roca fosfórica que contiene P2 O5 en la fosforita Ca3 (PO4)2. Los huesos y dientes contienen este elemento.
Tiene aplicaciones para la elaboración de detergentes, plásticos, lacas, pinturas, alimentos para ganado y aves.
Fósforo
El fósforo lo descubrió por primera vez, en 1669, el alquimista alemán, nacido en Hamburgo, Henning Brandt. El método de obtención partía de grandes cantidades de orines dejados descomponer durante largo tiempo. Después se destilaban, condensándose los vapores en agua. Se obtenía así un producto blando que en la oscuridad irradiaba luz.
Molécula de fósforo.
Este extraño fenómeno causó la lógica sensación allí donde se mostraba. Fue, por tanto, el primer elemento aislado a partir de un material biológico.
En 1833 la sociedad occidental descubrió lo fácil que era producir una llama utilizando cerillas de fósforo blanco. Sin embargo, cientos de mujeres que trabajaban en las fábricas de cerillas murieron debido a la extrema toxicidad del fósforo blanco.
Su nombre deriva de las palabras griegas phos (luz) y phorus (portador); el fósforo es el portador de luz.
El interior de una lámpara fluorescente, por ejemplo, está recubierto con fósforo, sustancia química que absorbe la luz ultravioleta invisible y emite luz visible.
Punto de fusión: 44,15° C
Punto de ebullición: 280,5° C
El fósforo no se encuentra en estado libre en la naturaleza debido a su gran afinidad por el oxígeno con el que forma un gran número de compuestos.
Su estructura es cristalina. La partícula elemental de sus compuestos está constituida por un átomo central de fósforo rodeado de cuatro átomos de oxigeno en el caso de los fosfatos. Si el átomo central es de arsénico se formarán los arseniatos, y si es de vanadio lo harán los vanadatos.
Esta clase mineralógica está constituida en su mayor parte por fosfatos, aunque muchos de ellos son raros. El apatito, uno de estos fosfatos, representa el 95 por ciento de todo el fósforo existente en la corteza terrestre.
Se encuentra también en estado combinado en los suelos fértiles y en muchas aguas minerales.
El fósforo (P) se presenta en distintas variedades (alótropos) que difieren bastante en sus propiedades. Las dos variedades más importantes son el fósforo rojo y el fósforo blanco.
El fósforo ordinario es un sólido blanco céreo; cuando es puro es incoloro y transparente.
No se disuelve en el agua ni en el alcohol, pero es soluble en sulfuro de carbono, benceno, aceites vegetales, amoníaco líquido y éter.
Tanto el sólido como sus vapores son muy venenosos por lo que debe manejarse con mucho cuidado.
El fósforo blanco es muy activo y se combina con la mayor parte de los elementos. Arde en el oxígeno con una llama blanca muy brillante produciendo nubes de óxido de fósforo sólido. Aproximadamente a 50º C se produce su inflamación.
Otra forma del apatito.
Expuesto al aire se oxida lentamente y produce el fenómeno de la fosforescencia, que se observa en la oscuridad. Se produce con bastante frecuencia la inflamación espontánea del fósforo blanco, por lo que suele guardarse bajo el agua.
El fósforo rojo es menos reactivo que el blanco, y no se oxida fácilmente con el aire. Su temperatura de inflamación ronda los 400º C. No se disuelve en los mismos disolventes que el fósforo blanco ni produce fosforescencia ni resulta venenoso cuando se encuentra puro.
Utilidad del fósforo
El fósforo no sólo se emplea como fertilizante. La importancia de esta sustancia va creciendo de año en año. En la actualidad, se utiliza este "fuego frío", como mínimo, en 120 ramas de la industria.
Antes de todo, el fósforo es la sustancia básica de la vida y del pensamiento. El contenido de fósforo en los huesos determina el crecimiento y desarrollo normal de las células de la médula ósea y, en resumidas cuentas, es el que implica solidez a los organismos vivos.
Los huesos están formados en su mayoría por fosfato de calcio Ca3(PO4)2.
El contenido elevado de fósforo en la sustancia medular demuestra el papel importantísimo que desempeña para el trabajo funcional del cerebro.
Fósforo blanco en las municiones.
La falta de alimentación fosfórica conduce al debilitamiento de todo el organismo. No en vano existe gran número de medicamentos y preparados farmacéuticos a partir de fósforo, destinados a restablecer a los enfermos débiles o convalecientes. En las manzanas encontramos sodio, potasio, magnesio y fósforo.
El fósforo le necesitan, no sólo el hombre, sino también las plantas y animales en grandes cantidades. Hemos aprendido a abonar con fertilizantes fosfóricos, no sólo la tierra, sino también el mar.
En las bahías cerradas y en los golfos, la fertilización del agua del mar con fósforo, acrecienta considerablemente la multiplicación y crecimiento de algas diminutas y otros organismos microscópicos, lo que conduce a una reproducción intensa de los peces.
En los últimos tiempos, el fósforo ha adquirido suma importancia en la preparación de diversos productos alimenticios, especialmente, para las aguas minerales. Aguas minerales de alta calidad se obtienen con ayuda del ácido fosfórico. (Ver: Ciclo del fósforo)
Con sales de los ácidos fosfóricos, sobre todo las de manganeso y hierro, se fabrican excelentes materiales de recubrimiento, dotados de gran estabilidad.
Los mejores artículos de acero inoxidable se obtienen recubriéndolos con sales fosfóricas. Las superficies de los aviones pueden hacerse inoxidables empleando revestimientos fosfóricos.
El clásico "fósforo" o cerillo.
El "fuego frío" del fósforo en otros tiempos ha creado una de las ramas más importantes de la industria, la fabricación de cerillas.
De seguro, los jóvenes estudiantes de hoy no han conocido las cerillas de fósforo que se usaban antes de ser inventadas las actuales. Antaño, eran comunes las cerillas con cabeza roja, cuya base era el fósforo, que se encendían frotándolas en cualquier objeto.
Típica y famosa resulataba la escena del vaquero del oeste que la encendía raspándolas en la suela de los zapatos. Sin embargo, las cualidades peligrosas del fósforo obligaron a orientar otro tipo de cerillas como las que usamos actualmente.
(Ver: Historia de la cerilla o fósforo).
Una empresa canadiense creó una pantalla HDTV que usa tecnología basada en fósforo y que alcanza las 37 pulgadas de tamaño, tiene dos centímetros de grosor y pesa menos de un kilo.
Mercurio (Hg): Metal líquido a temperatura ambiente, de calor blanco brillante, resistente a la corrosión y buen conductor eléctrico. Se le emplea en la fabricación de instrumentos de precisión, baterías, termómetros, barómetros, amalgamas dentales, sosa cáustica, medicamentos, insecticidas y funguicidas y bactericidas.
Se le obtiene principalmente del cinabrio que contiene HgS.
Plata (Ag): Metal de color blanco, su uso principal ha sido el la acuñación de monedas y manufacturas de vajillas y joyas. Se emplea en fotografía, aparatos eléctricos, aleaciones, soldaduras.
Plomo (Pb): Metal blando de bajo punto de fusión, bajo límite elástico, resistente a la corrosión, se le obtiene del sulfuro llamado galena Pbs. Se usa en baterías o acumuladores, pigmentos de pinturas, linotipos. Soldaduras e investigaciones atómicas. Otros productos que se pueden recuperar de los minerales que lo contiene son: cadmio, cobre, oro, plata, bismuto, arsénico, telurio y antimonio.
Oro (Au): Metal de color amarillo, inalterable, dúctil, brillante, por sus propiedades y su rareza le hace ser excepcional y de gran valor. Es el patrón monetario internacional. En la naturaleza se encuentra asociado al platino, a la plata y teluro en unos casos. Sus aleaciones se emplean en joyería y ornamentos, piezas dentales, equipos científicos de laboratorio. Recientemente se ha sustituido sus usos en joyería por el iridio y el rutenio, en piezas dentales por platino y paladio.
Uranio (U): Utilizado como combustible nuclear, es un elemento raro en la naturaleza y nunca se presenta en estado libre. Existen 150 minerales que lo contienen. El torio se encuentra asociado al uranio.
Propiedades específicas de la materia
3.2.1Densidad de un cuerpo
Definición: La densidad (d) es la relación que existe entre la masa que tiene un cuerpo y el volumen que ocupa dicho cuerpo.
Matemáticamente se expresa mediante la siguiente expresión:
d = m/V y se mide en kg/m3en el SI.
Dónde d es la densidad, m es la masa y V es el volumen.
La densidad de un cuerpo es una propiedad tan importante que determina la flotabilidad de los cuerpos en diferentes líquidos.
Un cuerpo flota en un líquido si la densidad del cuerpo es menor que la del líquido. En caso contrario el cuerpo se hunde. Si ambos tuviesen la misma densidad, el sólido se quedaría flotando en cualquier punto del interior del líquido.Para medir la densidad de los líquidos se utilizan los densímetros . Son tubos graduados que poseen un peso en su parte inferior. Se sumergen en el líquido cuya densidad se desea conocer y la profundidad a la que se sumerge nos permite leer en la escala, directamente, la densidad del líquido, siempre de manera que el ojo esté situado a la misma altura que el nivel del líquido. |
4.- Estados de la materia
La materia se puede presentar en tres estados de agregación diferentes: sólido, líquido y gaseoso. Las propiedades de estos tres estados pueden explicarse mediante la teoría cinética.
| Definición: La teoría cinética supone que la materia está formada por partículas que se encuentran en continuo movimiento. Teoría Cinética de la materia : En el estado sólido las partículas se encuentran mucho más unidas que en el estado líquido y, en este estado, a su vez, mucho más juntas que en el estado gaseoso , en el que están muy alejadas y en un movimiento que es continuo, desordenado, caótico (gas en griego significa «caos»). De esta forma se explican las propiedades de los tres estados:
Los sólidos y los líquidos son prácticamente incompresibles , es decir, no pueden disminuir su volumen . Sin embargo, los gases sí pueden aumentar su volumen, por lo que son compresibles y expansibles . | ||

Estados de agregación del agua: Sólido: hielo
| 
Líquido: "Agua"
| 
Gaseoso: Vapor de agua (no nubes)
|
El volumen de una sustancia disminuye al bajar la temperatura, con lo que la densidad aumenta cuando se enfría. Así, el aceite sólido baja al fondo por tener una densidad más alta que el aceite líquido. Sin embargo, existe una importante excepción. Cuando el agua se enfría, su volumen disminuye, pero al llegar a 4° C ocurre lo contrario, su volumen aumenta, transformándose en hielo a 0 º C. Al ser el hielo menos denso que el agua, flota en ella. Gracias a esta anomalía, el agua comienza a congelarse desde la superficie, lo que hace que los seres acuáticos sobrevivan a pesar de las bajas temperaturas ambientales, pues el hielo a 0° C los protege térmicamente del exterior.
5 .- Cambios de estado
La materia puede variar su estado de agregación dependiendo, entre otros factores, de la temperatura.
Los cambios de estado que ocurren en la materia pueden ser progresivos , con aumento de la temperatura, o regresivos , con disminución de la temperatura. Mientras ocurre un cambio de estado, la temperatura permanece constante.
DEFINICIONES:
El punto de fusión de una sustancia es la temperatura a la cual el sólido pasa al estado líquido.
El punto de ebullición de una sustancia es la temperatura a la cual el líquido pasa al estado gaseoso por ebullición..
Ojo: Evaporación : es un proceso lento y ocurre a cualquier temperatura.
Ebullición : es un proceso violento. Todas las partículas del líquido quieren escapar a la superficie y ocurre siempre a una temperatura dada. El punto de ebullición .

La sublimación es el paso directo de sólido a gas (sublimación progresiva) o de gas a sólido (sublimación regresiva), sin pasar por el estado líquido.
6. Enlaces de interés.
http://recursostic.educacion.es/newton/web/
Proyecto Newton. En el proyecto Newton se desarrollan los temas de Física del currículo de la ESO y de Bachillerato a partir de simulaciones interactivas que permiten a los alumnos acercarse a conceptos complejos de forma intuitiva. Mediante el control de las distintas variables se obtienen diferentes resultados y se propone al alumno que indague, reflexione, formule hipótesis y las contraste.
Los materiales están agrupados en unidades didácticas, pero también por conceptos, cada uno ilustrado con una animación. Así el profesor puede acceder a objetos de aprendizaje modulares y utilizarlos con sus alumnos cuando en su programación considere que el uso del ordenador lo ayuda a mejorar su trabajo en el aula.
Puedes descargar el programa y usarlo en tu ordenador. Puedes descarte una imagen .iso, para grabarlo en un dvd y trabajar en tu propio ordenador.
Proyecto Newton. En el proyecto Newton se desarrollan los temas de Física del currículo de la ESO y de Bachillerato a partir de simulaciones interactivas que permiten a los alumnos acercarse a conceptos complejos de forma intuitiva. Mediante el control de las distintas variables se obtienen diferentes resultados y se propone al alumno que indague, reflexione, formule hipótesis y las contraste.
Los materiales están agrupados en unidades didácticas, pero también por conceptos, cada uno ilustrado con una animación. Así el profesor puede acceder a objetos de aprendizaje modulares y utilizarlos con sus alumnos cuando en su programación considere que el uso del ordenador lo ayuda a mejorar su trabajo en el aula.
Puedes descargar el programa y usarlo en tu ordenador. Puedes descarte una imagen .iso, para grabarlo en un dvd y trabajar en tu propio ordenador.
http://concurso.cnice.mec.es/cnice2005/93_iniciacion_interactiva_materia/curso/materiales/indice.htm
Permite trabajar con los conceptos de masa, volumen, densidad, estados de la materia y cambios de estado
Permite trabajar con los conceptos de masa, volumen, densidad, estados de la materia y cambios de estado
http://www.iesaguilarycano.com/dpto/fyq/recursos2.html
Numerosos recursos para la enseñanza de Física y Química elaborados por el profesorado del departamento del IES Aguilar y Cano.
Numerosos recursos para la enseñanza de Física y Química elaborados por el profesorado del departamento del IES Aguilar y Cano.
http://www.juntadeandalucia.es/averroes/recursos_informaticos/concurso1999/accesit3/index.htm
Más sobre la materia
Más sobre la materia
http://www.araucaria2000.cl/sinternacional/sinternacional.php
Facilita el estudio de las unidades de medida y las transformaciones entre ellas.
Facilita el estudio de las unidades de medida y las transformaciones entre ellas.
http://www.araucaria2000.cl/quimica/quimica.htm
Contiene información sobre el estudio de la materia y los cambios de estado. Estas dos últimas son de paises hispano americanos. Algunos nombres o palabras pueden cambiar de su español al nuestro.
Contiene información sobre el estudio de la materia y los cambios de estado. Estas dos últimas son de paises hispano americanos. Algunos nombres o palabras pueden cambiar de su español al nuestro.
----------------------------------------------------------------------------------------------------------------------------------
Tema 2. Estructura de la materia. |
1.- Átomos y moléculas
| Definición: En química y física, átomo (del latín atomus , y éste del griego " Los griegos llamaron átomo a la parte más pequeña de materia que no se puede dividir en otras partes. Sin embargo hay otras partículas más pequeñas que forman los átomos que son los protones , losneutrones y los electrones . ¿Cómo es un átomo? El átomo está formado por una zona central llamada núcleo , en el que se encuentran los protones y los neutrones . En torno a él se encuentra una zona denominada corteza , con los electrones girando en diferentes órbitas. |  |
| Aunque te parezca increíble, electrones, protones y neutrones también están formados de partículas más pequeñas: los quarks. Son un tipo de partículas elementales, componentes de otras partículas subatómicas, como el protón y el neutrón, y que no existen de manera aislada | |
 Se muestra la estructura del quark en un neutrón, dos quark abajo (down) y un quark arriba (up) |  Se muestra la estructura de un quark en un protón dos quark arriba y un quark abajo |
| Para saber más pincha aquí | |
Cuando los átomos se unen entre sí pueden formar:
| • Moléculas : unión de varios átomos, iguales o distintos, en número concreto. | • Redes cristalinas : unión de un número indefinido de átomos de una forma ordenada en las tres dimensiones del espacio. |
 |  |
Existen muchos tipos de átomos, dependiendo del número de partículas subatómicas que posean. El conjunto de muchos átomos con el mismo número de protones es lo que constituye un elemento.
2.- Sustancias puras y mezclas.
La materia se presenta ante nuestros ojos en «porciones».
Llamamos sistemas materiales a todas estas porciones que podemos aislar para el estudio de sus propiedades
| “Definición: Cuerpo material es toda forma de materia que tiene límites propios bien definidos. | Definición: Sistema material Es toda forma de materia que carece de morfología (forma) propia o cuyos límites son imprecisos, ya sea por su naturaleza o por su extensión”. |
 Cuerpo material |  Sistema material |
Los sistemas materiales se encuentran formando mezclas, como el aire, o sustancias puras, como el azúcar o el oro.
| Las mezclas están formadas por dos o más sustancias puras que pueden separarse por procesos físicos (son cambios que no alteran la naturaleza de la materia). | Las sustancias puras están formadas por un solo componente, no pudiendo separarse en otros por procesos físicos. |
 Mezclas de rocas |  Oro puro |
Es difícil saber si una sustancia es pura o no a simple vista. Para comprobarlo tenemos que fijarnos en sus propiedades físicas (densidad, punto de fusión o ebullición, etc.).
Definición: Una sustancia pura tiene sus propiedades características bien definidas y constantes. Una mezcla no tiene propiedades definidas.
3.- Sustancias simples y compuestos
| Definición: Una sustancia simple es una sustancia pura que está formada por una sola clase de átomos. | Definición: Un compuesto es una sustancia pura formada por átomos diferentes. | ||
 Elemento. Sodio metálico |  Estructura de átomos de sodio |  Compuesto. Halita. ClNa. Sal común |  Estructura del ClNa |
Para saber si una sustancia pura es un elemento o un compuesto, basta con saber si puede descomponerse en otras sustancias más sencillas o no. Si puede descomponerse, es un compuesto ; en caso contrario, es un elemento .
Definición: Una reacción química es un proceso mediante el cual una o varias sustancias con unas propiedades definidas, denominadas reactivos , se transforman en otras sustancias con propiedades diferentes a las iniciales, denominadas productos .
2H 2O  2H2 + O2
2H2 + O2
Hay infinidad de sustancias puras. Cada sustancia se representa de manera simplificada mediante una fórmula química . Esta consta de los símbolos químicos (que representan deforma abreviada los elementos de la sustancia) y de unos subíndices que nos indican el número de átomos que existen en la molécula. La fórmula del agua es H2O, y quiere decir que en cada molécula de este compuesto hay dos átomos de hidrógeno (H) y un átomo de oxígeno (O).
4.- Elementos químicos en el universo
Todos los elementos que actualmente conocemos y que forman parte del universo están representados en el sistema periódico . Están colocados siguiendo un orden creciente al número de protones y electrones que tienen sus átomos.
Para ver el Sistema periódico pincha aquí
Cada elemento viene representado por su símbolo , que consta de una o dos letras. A veces el símbolo es la parte de su nombre en castellano, (Oxígeno, O; Magnesio, Mg) pero en otros es parte de nombre en latín o griego, (Sodio, Na de Natrum, Azufre, S de sulphur).
Estudiando las propiedades de los elementos del sistema periódico se puede hacer una clasificación muy general en:
• Metales . Son buenos conductores del calor y de la electricidad, en general, tienen puntos de fusión y ebullición altos y densidades altas.
• No metales : Son malos conductores, tienen puntos de fusión y ebullición bajos y poseen densidades bajas.
Es mejor es clasificar los elementos en grupos o familias , que se corresponden con cada una de las columnas del sistema periódico. Todos los elementos que forman una columna tienen propiedades muy parecidas.
Alcalinos, alcalinotérreos, térreos, carbonoideos, nitrogenoideos, calcógenos o anfígenos, halógenos y gases nobles. Metales pesados (transición), lantánidos y actínidos.
5. Tipos de mezclas
5.1. Mezclas heterogéneas
| Definición: Una mezcla es heterogénea cuando sus componentes pueden ser distinguidos a simple vista. | Definición: Una mezcla es homogénea cuando sus componentes no se pueden distinguir a simple vista. |
 |  Mezclas homogéneas. |
5.2.- Mezclas homogéneas. Disoluciones
Las mezclas homogéneas también se llaman disoluciones y están formadas por dos o más componentes. Pueden ser disoluciones de sólidos, líquidos y gases.
Definición: Soluto es el componente que se en cuentra en menor proporción en una disolución.
Definición: Disolvente es el componente que está mayor proporción en una disolución.
Tipos de disoluciones.
Las disoluciones pueden ser:
| • Diluidas si la cantidad de soluto es muy pequeña con relación a la cantidad de disolvente. | • Concentradas si la cantidad de soluto es muy alta en relación a la cantidad de disolvente. | • Saturada: Si no admite más soluto y si añadimos más este se queda en el fondo. |
 |  |  |
Definición: La concentración de una disolución es la cantidad de soluto que hay en una determinada cantidad de disolvente.
Se puede expresar en forma de porcentaje de masa : 20 % de masa sal en agua indica que hay 20 g de sal por cada 100g de disolución ( 80 g de agua). También se puede expresar en volumen : en g de soluto por litro de disolución (g/L).
6.- Separación de mezclas
Las técnicas de separación de una mezcla se basan en las diferentes propiedades físicas de sus componentes (densidad, punto de ebullición, etc.). Independientemente del tipo de mezcla, sus componentes se pueden separar a través de diversos métodos físicos .
6.1.- Técnicas de separación de mezclas homogéneas.
Los métodos más usados son: cristalización, destilación y la extracción para mezclas homogéneas , y Filtración, decantación y separación magnética para mezclas heterogéneas.
| Cristalización Se utiliza para separar un sólido disuelto en un líquido. Por ejemplo, si se tiene una disolución de agua y sal, y se deja evaporar el agua, aparecerán cristales de sal en el fondo. Si la evaporación es muy lenta, es posible que se formen unos bonitos cristales cúbicos de cloruro de sodio (sal común). | Destilación Esta técnica se emplea para separar líquidos que tienen puntos de ebullición muy diferentes o para separar los líquidos de impurezas sólidas que no se vaporizan. Por ejemplo, si se destila agua teñida con algún colorante, se obtiene en el destilado agua pura limpia (sin colorear) y en el matraz de destilación se queda el colorante. | Extracción Es una técnica basada en la diferente solubilidad que una sustancia tiene en dos líquidos inmiscibles, es decir, que no se pueden mezclar entre ellos. Por ejemplo, el yodo es muy poco soluble en agua, pero se disuelve muy bien en cloroformo. Si se tiene una disolución de yodo en agua, que es de color parda, y se quiere «extraer» el yodo de ella, basta con agitar la disolución con un poco de cloroformo. Así, la solución acuosa que era de color pardo queda incolora al pasar el yodo a teñir de rosa la disolución de cloroformo. |
 Cristalizaciones de disoluciones de agua con diferentes sales |  Destilación |  Extracción de Yodo disuelto en agua. |
6.2.- Técnicas de separación de mezclas heterogéneas.
Criba o tamizado
Si se quiere separar sólidos de diferentes tamaños, se puede pasar la mezcla a través de un tamiz.El sólido de mayor tamaño quedará retenido, mientras que el que tiene el grano más fino, pasará a través del tamiz. |
Filtración
Se utiliza para separar la mezcla de un líquido con un sólido que no se disuelve en ese líquido. Por ejemplo, si se pasa una mezcla de arena y agua a través de un filtro, la arena queda en el papel de filtro y en el líquido filtrado solo pasa el agua limpia. |
Sedimentación
Cuando hay un sólido en suspensión en el seno de un líquido, al dejarlo en reposo, por la acción de la gravedad, el sólido se deposita en el fondo. Por ejemplo, se puede emplear para separar la arcilla del agua. Se puede acelerar el proceso mediante una centrifugadora; la técnica, en este caso, se denomina centrifugación. |
 Tamizado. |  Filtros realizados con "papel de filtro" en laboretorio escolar. |  Sedimentación de diferentes solidos inmiscibles en agua. |
| Decantación Se emplea para separar líquidos inmiscibles, como por ejemplo el aceite y el agua. Para ello se utiliza el embudo de decantación. Accionando la llave del embudo se deja pasar el líquido más denso y en el interior del embudo queda el líquido menos denso. | Separación magnética Se usa cuando en una mezcla existen sustancias con propiedades magnéticas. Basta con pasar un imán para que las sustancias con propiedades magnéticas se separen de las que no las tienen. Este proceso se utiliza, por ejemplo, en las plantas de reciclaje. |
 Decantación. |  Separación magnética. |
La tensión superficial:
En un fluido cada molécula interacciona con las que le rodean. El radio de acción de las fuerzas moleculares es relativamente pequeño, abarca a las moléculas vecinas más cercanas. Vamos a determinar de forma cualitativa, la resultante de las fuerzas de interacción sobre una molécula que se encuentra en
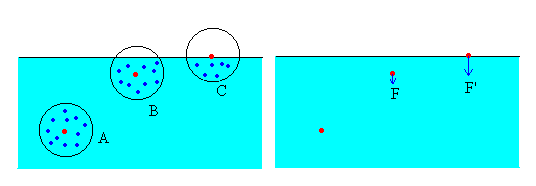
Consideremos una molécula (en color rojo) en el seno de un líquido en equilibrio, alejada de la superficie libre tal como la A. Por simetría, la resultante de todas las fuerzas atractivas procedentes de las moléculas (en color azul) que la rodean, será nula.
En cambio, si la molécula se encuentra en B, por existir en valor medio menos moléculas arriba que abajo, la molécula en cuestión estará sometida a una fuerza resultante dirigida hacia el interior del líquido.
Si la molécula se encuentra en C, la resultante de las fuerzas de interacción es mayor que en el caso B.
La fuerzas de interacción, hacen que las moléculas situadas en las proximidades de la superficie libre de un fluido experimenten una fuerza dirigida hacia el interior del líquido.
Como todo sistema mecánico tiende a adoptar espontáneamente el estado de más baja energía potencial, se comprende que los líquidos tengan tendencia a presentar al exterior la superficie más pequeña posible.
La fuerza F es independiente de la longitud x de la lámina. Si desplazamos el alambre deslizante una longitud Dx, las fuerzas exteriores han realizado un trabajo FDx, que se habrá invertido en incrementar la energía interna del sistema. Como la superficie de la lámina cambia en DS=2dDx (el factor 2 se debe a que la lámina tiene dos caras), lo que supone que parte de las moléculas que se encontraban en el interior del líquido se han trasladado a la superficie recién creada, con el consiguiente aumento de energía.
Si llamamos a g la energía por unidad de área, se verificará que

la energía superficial por unidad de área o tensión superficial se mide en J/m2 o en N/m.
La tensión superficial depende de la naturaleza del líquido, del medio que le rodea y de la temperatura. En general, la tensión superficial disminuye con la temperatura, ya que las fuerzas de cohesión disminuyen al aumentar la agitación térmica. La influencia del medio exterior se comprende ya que las moléculas del medio ejercen acciones atractivas sobre las moléculas situadas en la superficie del líquido, contrarrestando las acciones de las moléculas del líquido.
Tensión superficial de los líquidos a 20ºC
Fuente: Manual de Física, Koshkin N. I. , Shirkévich M. G.. Editorial Mir (1975)
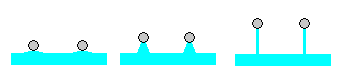
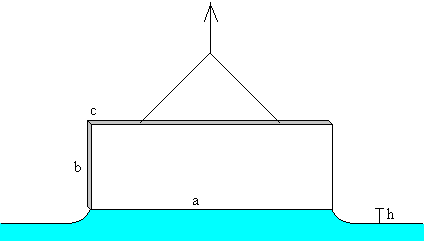
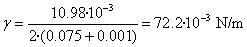
En un fluido cada molécula interacciona con las que le rodean. El radio de acción de las fuerzas moleculares es relativamente pequeño, abarca a las moléculas vecinas más cercanas. Vamos a determinar de forma cualitativa, la resultante de las fuerzas de interacción sobre una molécula que se encuentra en
- A, el interior del líquido
- B, en las proximidades de la superficie
- C, en la superficie

Consideremos una molécula (en color rojo) en el seno de un líquido en equilibrio, alejada de la superficie libre tal como la A. Por simetría, la resultante de todas las fuerzas atractivas procedentes de las moléculas (en color azul) que la rodean, será nula.
En cambio, si la molécula se encuentra en B, por existir en valor medio menos moléculas arriba que abajo, la molécula en cuestión estará sometida a una fuerza resultante dirigida hacia el interior del líquido.
Si la molécula se encuentra en C, la resultante de las fuerzas de interacción es mayor que en el caso B.
La fuerzas de interacción, hacen que las moléculas situadas en las proximidades de la superficie libre de un fluido experimenten una fuerza dirigida hacia el interior del líquido.
Como todo sistema mecánico tiende a adoptar espontáneamente el estado de más baja energía potencial, se comprende que los líquidos tengan tendencia a presentar al exterior la superficie más pequeña posible.
Coeficiente de tensión superficial
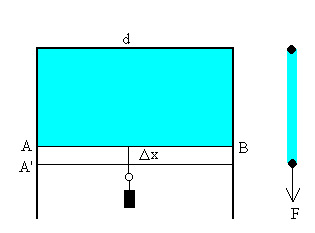 | Se puede determinar la energía superficial debida a la cohesión mediante el dispositivo de la figura.Una lámina de jabón queda adherida a un alambre doblada en doble ángulo recto y a un alambre deslizante AB. Para evitar que la lámina se contraiga por efecto de las fuerzas de cohesión, es necesario aplicar una fuerza F al alambre deslizante. |
Si llamamos a g la energía por unidad de área, se verificará que
la energía superficial por unidad de área o tensión superficial se mide en J/m2 o en N/m.
La tensión superficial depende de la naturaleza del líquido, del medio que le rodea y de la temperatura. En general, la tensión superficial disminuye con la temperatura, ya que las fuerzas de cohesión disminuyen al aumentar la agitación térmica. La influencia del medio exterior se comprende ya que las moléculas del medio ejercen acciones atractivas sobre las moléculas situadas en la superficie del líquido, contrarrestando las acciones de las moléculas del líquido.
Tensión superficial de los líquidos a 20ºC
| Líquido | g (10-3 N/m) |
| Aceite de oliva | 33.06 |
| Agua | 72.8 |
| Alcohol etílico | 22.8 |
| Benceno | 29.0 |
| Glicerina | 59.4 |
| Petróleo | 26.0 |
Medida de la tensión superficial de un líquido
El método de Du Nouy es uno de los más conocidos. Se mide la fuerza adicional ΔF que hay que ejercer sobre un anillo de aluminio justo en el momento en el que la lámina de líquido se va a romper.
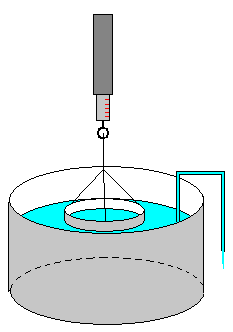 |
La tensión superficial del líquido se calcula a partir del diámetro 2R del anillo y del valor de la fuerza ΔF que mide el dinamómetro.
El líquido se coloca en un recipiente, con el anillo inicialmente sumergido. Mediante un tubo que hace de sifón se extrae poco a poco el líquido del recipiente.
|
En la figura se representa:

- El comienzo del experimento
- Cuando se va formando una lámina de líquido.
- La situación final, cuando la lámina comprende únicamente dos superficies (en esta situación la medida de la fuerza es la correcta) justo antes de romperse.
Si el anillo tiene el borde puntiagudo, el peso del líquido que se ha elevado por encima de la superficie del líquido sin perturbar, es despreciable.
No todos los laboratorios escolares disponen de un anillo para realizar la medida de la tensión superficial de un líquido, pero si disponen de portaobjetos para microscopio. Se trata de una pequeño pieza rectangular de vidrio cuyas dimensiones son a=75 mm de largo, b=25 mm de ancho y aproximadamente c=1 mm de espesor, su peso es aproximadamente 4.37 g.

Se pesa primero el portaobjetos en el aire y a continuación, cuando su borde inferior toca la superficie del líquido. La diferencia de peso ΔF está relacionada con la tensión superficial
ΔF=2·γ(a+c)
Se empuja el portaobjetos hacia arriba cuasiestáticamente. Justamente, cuando va a dejar de tener contacto con la superficie del líquido, la fuerza F que hemos de ejercer hacia arriba es igual a la suma de:
- El peso del portaobjetos mg
- La fuerza debida a la tensión superficial de la lámina de líquido que se ha formado 2·γ(a+c)
- El peso del líquido ρgach que se ha elevado una altura h, sobre la superficie libre de líquido. Siendo ρ es la densidad del líquido.
Para un portaobjetos de la dimensiones señaladas, que toca la superficie del agua, h es del orden de 2.3 mm (véase el artículo citado en las referencias)
- La fuerza debida a la tensión superficial es 2·γ(a+c)=2·72.8·10-3·(0.075+0.001)=11.07·10-3 N
- El peso de la lámina de agua es del orden de ρgach=1000·9.8·0.075·0.001·0.0023=1.70·10-3 N
Para que la simulación sea lo más simple posible, no se ha tenido en cuenta el peso de la lámina de líquido que se eleva por encima de la superficie libre.
Actividades
El programa interactivo genera aleatoriamente el peso de un portaobjetos entre ciertos límites.
Se pulsa el botón titulado Nuevo
- Se pesa el portaobjetos en el aire, arrastrando con el puntero del ratón las flechas de color azul, rojo y negro, que marcan los gramos, décimas y centésimas de gramo respectivamente.
- Se elige el líquido en el control de selección titulado Líquidos
Se pulsa el botón titulado Medir
- Se pesa el portaobjetos cuya parte inferior toca la superficie del líquido
Se calcula la diferencia ΔF entre ambos pesos
Se calcula la tensión superficial γ a partir de la fórmula
ΔF=2·γ(a+c)
donde a=75 mm y c=1 mm
Se compara el valor calculado, con el proporcionado por el programa interactivo pulsando el botón titulado Respuesta.
Ejemplo:
Se pesa el portaobjetos en el aire, 4.27 g
Se pesa el portaobjetos cuando toca la superficie del líquido 5.39 g
Calculamos la diferencia de los dos pesos en N
ΔF=(5.39-4.27)·9.8/1000=10.98·10-3 N
Se despeja la tensión superficial





















No hay comentarios:
Publicar un comentario